उच्च माध्यमिक परीक्षा, 2025
SENIOR SECONDARY EXAMINATION, 2025
रसायन विज्ञान
CHEMISTRY
समय : 3 घंटे 15 मिनट
|
पूर्णांक : 56
Showing all questions
बहुविकल्पीय प्रश्न (i से xviii)
(1) निम्नलिखित प्रश्नों के सही विकल्प का चयन कीजिए और उनके उत्तर दीजिए।
(i)
MgSO4 के पूर्ण वियोजन के लिए
वैन्ट हॉफ कारक (i)
का मान है —
(अ) 1
(ब) 2
(स) 3
(द) 4
(अ) 1
(ब) 2
(स) 3
(द) 4
Answer ✅
सही विकल्प है —👉
(ब) 2 ✅
व्याख्या (Step by Step) 👉
MgSO4
का पूर्ण वियोजन (complete dissociation) पानी में ऐसे होता है:👉 MgSO4 → Mg2+ + SO42−
✅ यहाँ 1 सूत्र इकाई से 2 आयन बनते हैं, इसलिए:
👉 वैन्ट हॉफ कारक (i) = 2
Did You Know? 🤔📌
✅
वैन्ट हॉफ कारक (i)
बताता है कि विलयन में
एक सूत्र इकाई
से कुल कितने
कण (आयन/अणु)
बन रहे हैं।
(ii)
प्रतिरोधकता (विशिष्ट प्रतिरोध) की
SI इकाई
है —
(अ) Ω
(ब) Ω·m−1
(स) Ω·m
(द) Ω·m−1
(अ) Ω
(ब) Ω·m−1
(स) Ω·m
(द) Ω·m−1
Answer ✅
सही विकल्प है —👉
(स) Ω·m ✅
व्याख्या (Step by Step) 👉
✅ प्रतिरोधकता / विशिष्ट प्रतिरोध
(ρ)
का सम्बन्ध होता है:👉 R = ρ (L/A)
यहाँ ρ = R(A/L)
• R की इकाई = Ω
• A की इकाई = m2
• L की इकाई = m
तो ρ की इकाई:
👉 Ω × (m2/m) = Ω·m
✅ इसलिए प्रतिरोधकता की SI इकाई Ω·m होती है।
Did You Know? 🤔📌
✅
प्रतिरोध (R)
वस्तु के
आकार
पर निर्भर करता है, लेकिन
प्रतिरोधकता (ρ)
केवल
पदार्थ (material)
की प्रकृति पर निर्भर करती है।
(iii)
गलित
सोडियम क्लोराइड
के
वैद्युतअपघटन
के उत्पाद हैं —
(अ) Na(s) एवं H2(g)
(ब) NaOH एवं H2SO4
(स) H2(g) एवं Cl2(g)
(द) Na(s) एवं Cl2(g)
(अ) Na(s) एवं H2(g)
(ब) NaOH एवं H2SO4
(स) H2(g) एवं Cl2(g)
(द) Na(s) एवं Cl2(g)
Answer ✅
सही विकल्प है —👉
(द) Na(s) एवं Cl2(g) ✅
व्याख्या (Step by Step) 👉
गलित (molten)
NaCl
में केवल
Na+
और
Cl−
आयन होते हैं
(पानी नहीं होता),
इसलिए उत्पाद ये बनते हैं:
कैथोड (−) पर: अपचयन (Reduction)
👉
Na+ + e− → Na(s)
✅ कैथोड पर सोडियम धातु बनती है।
एनोड (+) पर: ऑक्सीकरण (Oxidation)
👉
2Cl− → Cl2(g) + 2e−
✅ एनोड पर क्लोरीन गैस निकलती है।
✅ इसलिए कुल उत्पाद: Na(s) और Cl2(g)
Did You Know? 🤔📌
✅ गलित
NaCl
के वैद्युतअपघटन को
Downs process
कहा जाता है, जिससे औद्योगिक रूप से
सोडियम धातु
प्राप्त की जाती है।
(iv)
द्वितीय कोटि अभिक्रिया के लिए
वेग स्थिरांक (k)
की इकाई है —
(अ) s−1
(ब) mol L−1 s−1
(स) mol−1 L s−1
(द) mol−2 L2 s−1
(अ) s−1
(ब) mol L−1 s−1
(स) mol−1 L s−1
(द) mol−2 L2 s−1
Answer ✅
सही विकल्प है —👉
(स) mol−1 L s−1 ✅
व्याख्या (Step by Step) 👉
✅ सामान्यतः
वेग (Rate)
की इकाई होती है:👉 mol L−1 s−1
द्वितीय कोटि अभिक्रिया के लिए:
👉 Rate = k [A]2 (या k[A][B] )
अब [A] की इकाई = mol L−1
तो k की इकाई निकालें:
👉 k = (Rate) / ([A]2)
👉 k = (mol L−1 s−1) / (mol2 L−2)
👉 k = mol−1 L s−1
✅ इसलिए द्वितीय कोटि के वेग स्थिरांक की इकाई: mol−1 L s−1
Did You Know? 🤔📌
✅
n-th order reaction
के लिए
k
की इकाई बदलती रहती है, क्योंकि k की इकाई हमेशा
order
पर depend करती है।
(v)
ऐक्टिनॉइड श्रेणी का तत्व है —
(अ) थोरियम
(ब) सीरियम
(स) कैडमियम
(द) क्रोमियम
(अ) थोरियम
(ब) सीरियम
(स) कैडमियम
(द) क्रोमियम
Answer ✅
सही विकल्प है —👉
(अ) थोरियम ✅
व्याख्या (Step by Step) 👉
✅
थोरियम (Th, Z = 90)
ऐक्टिनॉइड श्रेणी
का तत्व है।
ऐक्टिनॉइड श्रेणी में सामान्यतः Ac (89) से Lr (103) तक के तत्व माने जाते हैं।
बाकी विकल्प:
• सीरियम (Ce) → लैन्थेनॉइड
• कैडमियम (Cd) → d-ब्लॉक तत्व
• क्रोमियम (Cr) → d-ब्लॉक संक्रमण तत्व
✅ इसलिए सही उत्तर थोरियम है।
क्या आप जानते हैं? 🤔📌
✅
ऐक्टिनॉइड तत्वों
में अधिकतर
रेडियोधर्मी (radioactive)
होते हैं।
✅ थोरियम का उपयोग नाभिकीय ऊर्जा (nuclear fuel research) में भी महत्वपूर्ण माना जाता है।
(vii)
होमोलेप्टिक संकुल है —
(अ) [Co(NH3)5Cl]2+
(ब) [Co(NH3)4Cl2]+
(स) [CoCl2(en)2]+
(द) [Co(NH3)6]3+
(अ) [Co(NH3)5Cl]2+
(ब) [Co(NH3)4Cl2]+
(स) [CoCl2(en)2]+
(द) [Co(NH3)6]3+
Answer ✅
सही विकल्प है —👉
(द) [Co(NH3)6]3+ ✅
व्याख्या (Step by Step) 👉
✅
होमोलेप्टिक (Homoleptic) संकुल
वह होता है जिसमें
सभी ligand एक ही प्रकार
के हों।
अब विकल्प देखें:
(अ) [Co(NH3)5Cl]2+ → NH3 और Cl, दो प्रकार के ligand ❌
(ब) [Co(NH3)4Cl2]+ → NH3 और Cl, दो प्रकार के ligand ❌
(स) [CoCl2(en)2]+ → Cl और en, दो प्रकार के ligand ❌
(द) [Co(NH3)6]3+ → केवल NH3 ligand ✅
✅ इसलिए सही उत्तर होमोलेप्टिक संकुल है:
👉 [Co(NH3)6]3+
क्या आप जानते हैं? 🤔📌
✅ जिस संकुल में
एक से अधिक प्रकार के ligand
हों, उसे
हेटेरोलेप्टिक (Heteroleptic) संकुल
कहते हैं।
✅ en (ethylenediamine) एक द्विदंती (bidentate) ligand है।
(viii)
[Cr(NH3)3(H2O)3]Cl3 संकुल में Cr की उपसहसंयोजन संख्या (coordination number) है —
(अ) 3
(ब) 9
(स) 5
(द) 6
(अ) 3
(ब) 9
(स) 5
(द) 6
Answer ✅
सही विकल्प है —👉
(द) 6 ✅
व्याख्या (Step by Step) 👉
✅
उपसहसंयोजन संख्या (Coordination number)
=
केंद्रीय धातु से सीधे जुड़े दाता परमाणु (लिगैण्ड) की कुल संख्या।
दिया गया संकुल:
👉 [Cr(NH3)3(H2O)3]Cl3
यहाँ bracket के अंदर वाले ligands ही Cr से जुड़े हैं:
🤔 NH3 = 3 (एकदन्तुक लिगैण्ड)
🤔 H2O = 3 (एकदन्तुक लिगैण्ड)
कुल लिगैण्ड = 3 + 3 = 6
✅ इसलिए Cr की उपसहसंयोजन संख्या = 6
ध्यान दें:
🤔 बाहर के 3Cl− आयन हैं, ये उपसहसंयोजन मण्डल (coordination sphere) के बाहर हैं ❌
🤔 इसलिए इन्हें उपसहसंयोजन संख्या में नहीं गिना जाता।
क्या आप जानते हैं? 🤔📌
✅
उपसहसंयोजन संख्या 6
होने पर संकुल की ज्यामिति अक्सर
अष्ठफलकीय
होती है।
✅ NH3 और H2O दोनों उदासीन लिगैण्ड हैं।
(ix)
थायोनिल क्लोराइड है —
(अ) SOCl2
(ब) SO2Cl2
(स) COCl2
(द) SOCl3
(अ) SOCl2
(ब) SO2Cl2
(स) COCl2
(द) SOCl3
Answer ✅
सही विकल्प है —👉
(अ) SOCl2 ✅
व्याख्या (Step by Step) 👉
✅
थायोनिल क्लोराइड (Thionyl chloride)
का रासायनिक सूत्र
SOCl2
होता है।
बाकी विकल्प:
• SO2Cl2 → सल्फ्यूरिल क्लोराइड (Sulfuryl chloride)
• COCl2 → फॉस्जीन (Phosgene)
• SOCl3 → थायोनिल क्लोराइड नहीं है
✅ इसलिए सही उत्तर SOCl2 है।
क्या आप जानते हैं? 🤔📌
✅
SOCl2
का उपयोग
alcohols से alkyl chlorides
तथा
carboxylic acids से acid chlorides
बनाने में किया जाता है।
✅ इसकी अभिक्रिया में अक्सर SO2 और HCl गैसें निकलती हैं, जो reaction mixture से बाहर निकल जाती हैं।
(x)
बैंज़िलिक हैलाइड में हैलोजन परमाणु से जुड़े कार्बन परमाणु की संकरित अवस्था है —
(अ) sp
(ब) sp2
(स) sp3
(द) sp3d
(अ) sp
(ब) sp2
(स) sp3
(द) sp3d
Answer ✅
सही विकल्प है —👉
(स) sp3 ✅
व्याख्या (Step by Step) 👉
✅
बैंज़िलिक हैलाइड (Benzylic halide)
में हैलोजन
बेंजीन रिंग से सीधे जुड़े कार्बन
पर नहीं, बल्कि
रिंग के पास वाले (benzylic) कार्बन
पर लगा होता है।
उदाहरण:
👉 C6H5–CH2Cl (benzyl chloride)
यहाँ हैलोजन जिस कार्बन से जुड़ा है, वह –CH2– carbon है।
इस कार्बन पर सामान्यतः 4 σ-bonds/regions होते हैं, इसलिए इसकी hybridisation:
👉 sp3
✅ इसलिए सही उत्तर sp3 है।
क्या आप जानते हैं? 🤔📌
✅
Aryl halide
में हैलोजन सीधे
बेंजीन रिंग के कार्बन
से जुड़ा होता है, वहाँ कार्बन की संकरण
sp2
होती है।
✅ बेंज़िलिक हेलाइड्स अनुनाद के कारण स्थायी होने से SN1/SN2 अभिक्रिया देते हैं।
(xi)
अधोलिखित में से असममित ईथर है —
(अ) CH3–O–CH3
(ब) C2H5–O–C2H5
(स) C6H5–O–C6H5
(द) C6H5–O–CH3
(अ) CH3–O–CH3
(ब) C2H5–O–C2H5
(स) C6H5–O–C6H5
(द) C6H5–O–CH3
Answer ✅
सही विकल्प है —👉
(द) C6H5–O–CH3 ✅
व्याख्या (Step by Step) 👉
✅ ईथर का सामान्य सूत्र होता है:
R–O–R′
✅ जब ऑक्सीजन के दोनों ओर एक जैसे समूह हों, तो उसे सममित ईथर (Symmetrical ether) कहते हैं।
उदाहरण:
👉 CH3–O–CH3
👉 C2H5–O–C2H5
✅ जब ऑक्सीजन के दोनों ओर अलग-अलग समूह हों, तो उसे असममित ईथर (Unsymmetrical ether) कहते हैं।
👉 C6H5–O–CH3 में एक ओर फिनाइल समूह (C6H5–) है और दूसरी ओर मिथाइल समूह (CH3–) है।
✅ इसलिए यह असममित ईथर है।
क्या आप जानते हैं? 🤔📌
✅
C6H5–O–CH3
को
एनीसोल (Anisole)
कहते हैं।
✅ एनीसोल एक aryl alkyl ether है, क्योंकि इसमें एक ओर एरिल (phenyl) और दूसरी ओर alkyl (methyl) समूह होता है।
✅ सममित ईथर में दोनों ओर same group होने से उनका नामकरण और पहचान आसान होती है।
(xii)
CH3–CH2–OH ⟶ (सांद्र H2SO4, 413 K) ⟶ [A]
उपर्युक्त अभिक्रिया में मुख्य उत्पाद [A] है —
(अ) CH3–O–CH3
(ब) C2H5–O–C2H5
(स) CH3–CH = CH2
(द) CH2 = CH2
उपर्युक्त अभिक्रिया में मुख्य उत्पाद [A] है —
(अ) CH3–O–CH3
(ब) C2H5–O–C2H5
(स) CH3–CH = CH2
(द) CH2 = CH2
Answer ✅
सही विकल्प है —👉
(ब) C2H5–O–C2H5 ✅
व्याख्या (Step by Step) 👉
✅ दिए गए अभिकारक में
एथेनॉल (CH3CH2OH)
है।
✅ सांद्र H2SO4 और 413 K पर एथेनॉल का अंतराअणुक निर्जलीकरण (intermolecular dehydration) होता है।
👉 इस प्रक्रिया में दो एथेनॉल अणु मिलकर डाइएथिल ईथर बनाते हैं:
2CH3CH2OH ⟶ CH3CH2–O–CH2CH3 + H2O
✅ इसलिए मुख्य उत्पाद [A] = डाइएथिल ईथर
👉 C2H5–O–C2H5
✅ अतः सही उत्तर (ब) है।
क्या आप जानते हैं? 🤔📌
✅
413 K
पर एथेनॉल से मुख्यतः
ईथर
बनता है।
✅ उच्च ताप (~443 K) पर वही एथेनॉल निर्जलीकरण करके एथीन (CH2=CH2) देता है।
✅ तापमान बदलने से alcohol की अभिक्रिया का उत्पाद बदल सकता है।
(xiii)
निम्नलिखित में से कौनसा ऐल्डिहाइड कैनिजारो अभिक्रिया देता है —
(अ) CH3–CHO
(ब) CH3–CH2–CHO
(स) (CH3)2–CH–CHO
(द) C6H5–CHO
(अ) CH3–CHO
(ब) CH3–CH2–CHO
(स) (CH3)2–CH–CHO
(द) C6H5–CHO
Answer ✅
सही विकल्प है —👉
(द) C6H5–CHO ✅
व्याख्या (Step by Step) 👉
✅
कैनिजारो अभिक्रिया (Cannizzaro reaction)
वे ऐल्डिहाइड देते हैं जिनमें
α-हाइड्रोजन (alpha hydrogen) नहीं होता।
✅ अब विकल्पों को देखें:
👉 (अ) CH3–CHO (एथेनैल)
इसमें α-कार्बन पर H मौजूद है।
❌ इसलिए कैनिजारो अभिक्रिया नहीं देगा।
👉 (ब) CH3–CH2–CHO (प्रोपेनैल)
इसमें भी α- कार्बन पर H मौजूद है।
❌ कैनिजारो अभिक्रिया नहीं देगा।
👉 (स) (CH3)2–CH–CHO
इसमें –CHO के पास वाले कार्बन (α-carbon) पर H मौजूद है।
❌ यह भी कैनिजारो अभिक्रिया नहीं देगा।
👉 (द) C6H5–CHO (बेंजैल्डिहाइड)
यहाँ –CHO के पास benzene ring carbon है, और उस कार्बन पर α-H नहीं होता।
✅ इसलिए यह कैनिजारो अभिक्रिया देता है।
✅ अतः सही उत्तर C6H5–CHO (बेंजैल्डिहाइड) है।
क्या आप जानते हैं? 🤔📌
✅
कैनिजारो अभिक्रिया
में एक ही ऐल्डिहाइड अणु का
ऑक्सीकरण
और दूसरे का
अपचयन
होता है
(disproportionation)।
✅ बेंजैल्डिहाइड सान्द्र क्षार (जैसे conc. NaOH/KOH) की उपस्थिति में बैंजिल एल्कोहोल और बैंजोएट लवण देता है।
✅ जिन ऐल्डिहाइड्स में α-H होता है, वे सामान्यतः एल्डोल संघनन की ओर जाते हैं, कैनिजारो की ओर नहीं।
(xv)
हिन्सबर्ग अभिकर्मक है —
(अ) C6H5SO2Cl
(ब) C6H5SO2Cl2
(स) C6H5SOCl2
(द) C6H5SO3Cl
(अ) C6H5SO2Cl
(ब) C6H5SO2Cl2
(स) C6H5SOCl2
(द) C6H5SO3Cl
Answer ✅
सही विकल्प है —👉
(अ) C6H5SO2Cl ✅
व्याख्या (Step by Step) 👉
✅
हिन्सबर्ग अभिकर्मक (Hinsberg reagent)
का नाम है:
👉 बेंजीनसल्फोनील क्लोराइड
इसका सूत्र होता है:
👉 C6H5SO2Cl
✅ इसका उपयोग 1° (प्राथमिक), 2° (द्वितीयक) और 3° (तृतीयक) एमीन में अंतर करने के लिए किया जाता है (Hinsberg test)।
इसलिए सही विकल्प:
✅ (अ) C6H5SO2Cl
क्या आप जानते हैं? 🤔📌
✅
Hinsberg test
में
प्राथमिक एमीन
से बना उत्पाद
क्षार में घुल सकता है,
जबकि
द्वितीयक एमीन
का उत्पाद सामान्यतः
नहीं घुलता।
✅ तृतीयक अमाइन बेंजीनसल्फोनील क्लोराइड से सामान्य परिस्थितियों में सल्फोनामाइड नहीं बनाता।
(xvi)
CH3–NH–CH2–CH3 का IUPAC नाम है —
(अ) प्रोपेन-1-एमीन
(ब) प्रोपेन-2-एमीन
(स) N-मेथिलएथेमीन
(द) N-एथिलमेथेमीन
(अ) प्रोपेन-1-एमीन
(ब) प्रोपेन-2-एमीन
(स) N-मेथिलएथेमीन
(द) N-एथिलमेथेमीन
Answer ✅
सही विकल्प है —👉
(स) N-मेथिलएथेमीन ✅
व्याख्या (Step by Step) 👉
✅ दिया गया यौगिक है:
CH3–NH–CH2–CH3
✅ इसमें नाइट्रोजन (N) से दो alkyl groups जुड़े हैं:
👉 एक मिथाइल (CH3–)
👉 एक एथाइल (CH3CH2–)
✅ ऐसे यौगिक को द्वितीयक अमाइन (2° अमाइन) कहते हैं।
IUPAC नाम कैसे बनेगा?
✅ लंबी कार्बन श्रृंखला को जनक मानते हैं, यानी ethanamine (एथेमीन) को जनक लिया जाएगा।
✅ नाइट्रोजन पर जुड़ा दूसरा समूह मिथाइल है, इसलिए N- prefix लगेगा।
👉 नाम होगा: N-methylethanamine
✅ हिंदी में यह N-मेथिलएथेमीन दिया है।
इसलिए सही विकल्प: (स) ✅
क्या आप जानते हैं? 🤔📌
✅
CH3NHCH2CH3
का सामान्य नाम:
एथिल मेथिल एमीन
भी कहा जाता है।
✅ प्राथमिक ऐमीन में N से एक ऐल्किल समूह, द्वितीयक ऐमीन में दो, और तृतीयक ऐमीन में तीन ऐल्किल समूह जुड़े होते हैं।
✅ IUPAC naming में N पर जुड़े प्रतिस्थापी को N- लिखकर दर्शाते हैं।
(xviii)
अनावश्यक एमीनो अम्ल है —
(अ) वेलीन
(ब) ल्यूसीन
(स) लाइसिन
(द) ग्लाइसिन
(अ) वेलीन
(ब) ल्यूसीन
(स) लाइसिन
(द) ग्लाइसिन
Answer ✅
सही विकल्प है —👉
(द) ग्लाइसिन ✅
व्याख्या (Step by Step) 👉
✅
एमीनो अम्ल (Amino acids)
को शरीर की आवश्यकता के आधार पर दो भागों में बाँटा जाता है:
1. आवश्यक (Essential) amino acids
👉 जिन्हें शरीर स्वयं नहीं बना सकता, इसलिए भोजन से लेने पड़ते हैं।
2. अनावश्यक (Non-essential) amino acids
👉 जिन्हें शरीर स्वयं बना सकता है।
अब विकल्प देखें 👇
👉 वेलीन (Valine) = आवश्यक अमीनो अम्ल ❌
👉 ल्यूसीन (Leucine) = आवश्यक अमीनो अम्ल ❌
👉 लाइसिन (Lysine) = आवश्यक अमीनो अम्ल ❌
👉 ग्लाइसिन (Glycine) = अनावश्यक अमीनो अम्ल ✅
✅ इसलिए सही उत्तर (द) ग्लाइसिन है।
क्या आप जानते हैं? 🤔📌
✅
ग्लाइसिन
सबसे सरल अमीनो अम्ल है, क्योंकि इसके
पार्श्व श्रृंखला
में केवल
H
होता है।
✅ ग्लाइसिन प्रकाशीय रूप से निष्क्रिय होता है (इसमें chiral carbon नहीं होता)।
✅ वेलीन, ल्यूसीन और लाइसिन जैसे अमीनो अम्ल शरीर की वृद्धि और प्रोटीन संश्लेषण में महत्वपूर्ण होते हैं।
(2) रिक्त स्थान भरें : (i से x)
(i)
हिमांक अवनमन स्थिरांक
(Kf)
की इकाई _______ है।
Answer ✅
👉
K kg mol−1
(या
K·kg·mol−1)
व्याख्या (Step by Step) 👉
क्योंकि👉 ΔTf = Kf × m
जहाँ molality (m) की इकाई = mol kg−1
इसलिए Kf की इकाई = K kg mol−1
Did You Know? 🤔📌
✅
Kf
को
molal depression constant
भी कहते हैं।
(ii)
सांद्रता घटने के साथ
मोलर चालकता
_______ है।
Answer ✅
👉
बढ़ती है / increases
व्याख्या (Step by Step) 👉
तनुता बढाने पर
आयनों की गतिशीलता
बढ़ती है और
अन्तरआयनिक आकर्षण
घटता है, इसलिए
मोलर चालकता
बढ़ती है।
Did You Know? 🤔📌
✅ बहुत अधिक तनु विलयन पर
molar conductivity
अपनी
limiting value
के पास पहुँचती है।
(iii)
उच्च दाब पर, गैसीय अमोनिया का गरम प्लेटिनम सतह पर विघटन _______ कोटि की अभिक्रिया का उदाहरण है।
Answer ✅
👉
शून्य (0th) कोटि / zero order
व्याख्या (Step by Step) 👉
गरम प्लेटिनम की सतह पर अभिक्रिया का वेग
surface saturation
के कारण अभिकारक की
सांद्रता
बदलने पर भी नहीं बदलता।इसलिए यह शून्य-कोटि अभिक्रिया कहलाती है।
Did You Know? 🤔📌
✅ कई
surface-catalysed reactions
में zero-order behaviour तब दिखता है जब catalyst surface पूरी तरह भर जाती है।
(iv)
वसा के हाइड्रोजनीकरण में _______ उत्प्रेरक के रूप में प्रयुक्त होता है।
Answer ✅
👉
निकेल (Ni)
व्याख्या (Step by Step) 👉
Fats के hydrogenation में सामान्य catalyst:
finely divided Ni
(कभी
Pt/Pd
भी), but standard answer
Ni
है।वसा (Fats) के हाइड्रोजनीकरण में सामान्य उत्प्रेरक (catalyst) बारीक विभाजित निकेल (Ni) होता है।
Did You Know? 🤔📌
✅ इसी प्रक्रिया से वनस्पति घी बनाने में
unsaturated fats
का hydrogenation किया जाता है।
(v)
Fe(CO)5 में आयरन की
ऑक्सीकरण अवस्था
_______ है।
Answer ✅
👉
0 (शून्य)
व्याख्या (Step by Step) 👉
CO
एक
उदासीन (neutral) ligand
होता है।पूरे complex का कुल आवेश 0 है, इसलिए Fe की oxidation state = 0 होगी।
Did You Know? 🤔📌
✅ Metal carbonyls जैसे
Fe(CO)5
में ligand charge पहचानना oxidation state निकालने की key trick है।
(vi)
मेथनॉल का
क्वथनांक
_______ K है।
Answer ✅
👉
338 K
(लगभग
337.8 K)
व्याख्या (Step by Step) 👉
Methanol का boiling point ≈
64.7°C
Kelvin में: 64.7 + 273 ≈ 338 K
Did You Know? 🤔📌
✅ Alcohols में
hydrogen bonding
होने से उनका boiling point समान molar mass वाले hydrocarbons से अधिक होता है।
(vii)
जब फिनॉल की अभिक्रिया सान्द्र नाइट्रिक अम्ल से कराई जाती है तो _______ उत्पाद बनता है।
Answer ✅
👉
2,4,6-ट्राइनाइट्रोफिनॉल (पिक्रिक अम्ल) / picric acid
व्याख्या (Step by Step) 👉
फिनोल एक
प्रबल सक्रियकारी समूह
(strong activating group) है। इसलिए
सान्द्र HNO3
के साथ nitration करने पर
2,4,6-ट्राइनाइट्रोफिनोल (पिक्रिक अम्ल)
बनता है।
Did You Know? 🤔📌
✅ फिनोल में
–OH group
ring को ortho/para positions पर बहुत अधिक activate करता है।
(viii)
H2SO4 एवं HgSO4 की उपस्थिति में एथाइन में जल योग से _______ प्राप्त होता है।
Answer ✅
👉
एथेनैल (एसीटैल्डिहाइड) / ethanal (acetaldehyde)
व्याख्या (Step by Step) 👉
एथाइन (Ethyne) का जलयोजन (hydration) जब
H2SO4/HgSO4
की उपस्थिति में किया जाता है, तो पहले
इनॉल (enol)
बनता है।यह इनॉल स्थायी नहीं होता, इसलिए टॉटोमेरीकरण (tautomerisation) होकर एथेनैल (ethanal / एसीटैल्डिहाइड) बनाता है।
Did You Know? 🤔📌
✅ यह reaction
Kucherov hydration
से जुड़ा हुआ concept है (alkyne hydration via Hg2+ catalyst)।
(ix)
विटामिन B एवं _______
जल में विलेय विटामिन
हैं।
Answer ✅
👉
विटामिन C
व्याख्या (Step by Step) 👉
Water-soluble vitamins:
B-complex and C
Did You Know? 🤔📌
✅ जल में विलेय vitamins शरीर में कम store होते हैं, इसलिए इन्हें diet से नियमित लेना चाहिए।
(x)
सुक्रोज का अपघटन (hydrolysis) ग्लूकोज तथा _______ देता है।
Answer ✅
👉
फ्रक्टोज / fructose
व्याख्या (Step by Step) 👉
👉
Sucrose + H2O → Glucose + Fructose
Did You Know? 🤔📌
✅ Sucrose hydrolysis से बनने वाला
glucose + fructose mixture
invert sugar
कहलाता है।✅ Fe(CO)5 जैसे compounds में metal की oxidation state निकालते समय ligand का charge ध्यान से देखना बहुत ज़रूरी होता है।
(3) अतिलघुत्तरात्मक प्रश्न: (i to x)
(निम्नलिखित प्रश्नों के उत्तर एक शब्द या एक पंक्ति में दीजिए)
(i)
मोललता
की परिभाषा लिखिए।
Answer ✅
✅
मोललता (Molality)
:
1 किलोग्राम विलायक (solvent)
में घुली हुई
विलेय (solute)
के
मोलों की संख्या
को विलयन की
मोललता (m)
कहते हैं।
👉 सूत्र: m = (विलेय के मोल) / (विलायक का द्रव्यमान किलोग्राम में)
व्याख्या (Step by Step) 👉
👉
विलेय
= जो पदार्थ घुलता है
👉 विलायक = जिसमें विलेय घुलता है
👉 मोललता आयतन पर नहीं, बल्कि द्रव्यमान पर आधारित होती है, इसलिए तापमान बदलने पर यह सामान्यतः नहीं बदलती।
क्या आप जानते हैं? 🤔📌
✅ मोललता की प्रचलित इकाई
मोल प्रति किलोग्राम
(mol kg−1)
होती है।
✅ अणुसंख्यक गुणधर्मों (जैसे क्वथनांक वृद्धि, हिमांक अवनमन) में मोललता का बहुत उपयोग होता है।
(ii)
राउल्ट के नियम
का
गणितीय रूप
लिखिए।
Answer ✅
✅
राउल्ट का नियम (Raoult’s Law)
का गणितीय रूप:
👉 PA = PA0 × XA
जहाँ,
• PA = विलयन में घटक A का आंशिक वाष्प दाब
• PA0 = शुद्ध घटक A का वाष्प दाब
• XA = घटक A का मोल अंश
व्याख्या (Step by Step) 👉
राउल्ट के नियम के अनुसार, किसी
आदर्श विलयन
में किसी
वाष्पशील घटक
का आंशिक वाष्प दाब, उसके
मोल अंश
के समानुपाती होता है।
यदि विलयन में विलेय अवाष्पशील हो, तो:
👉 P = P10 X1
और सापेक्ष वाष्प दाब अवनमन:
👉 (P0 − P) / P0 = X2
क्या आप जानते हैं? 🤔📌
✅
राउल्ट का नियम
आदर्श विलयनों
पर सबसे अच्छे से लागू होता है।
✅ इसी नियम के आधार पर अणुसंख्यक गुणधर्म (colligative properties) समझे जाते हैं।
(iii)
जटिल अभिक्रियाओं (Complex reactions)
को परिभाषित कीजिए।
Answer ✅
✅
जटिल अभिक्रियाएँ (Complex reactions)
वे अभिक्रियाएँ हैं जो
एक ही पद में पूरी नहीं होतीं,
बल्कि
दो या अधिक क्रमिक/समांतर प्राथमिक पदों (elementary steps)
में पूर्ण होती हैं।
व्याख्या (Step by Step) 👉
👉
सरल अभिक्रिया (simple reaction)
=
एक पद
में होती है।
👉 जटिल अभिक्रिया = कई छोटे-छोटे पदों में होती है।
👉 इन चरणों में मध्यवर्ती पदार्थ (intermediates) बन सकते हैं।
👉 कुल अभिक्रिया, इन सभी पदों का योगफल होती है।
✅ उदाहरण: N2O5 का विघटन दो पदों में होता है।
2N2O5 → 4NO2 + O2
क्या आप जानते हैं? 🤔📌
✅ जटिल अभिक्रिया की
overall order
हमेशा उसके
stoichiometric coefficients
से सीधे-सीधे नहीं निकाली जा सकती।
✅ कई बार अभिक्रिया की दर सबसे धीमे चरण (rate determining step) पर निर्भर करती है।
(iv)
K3[Cr(C2O4)3]
संकुल का
IUPAC नाम
लिखिए।
Answer ✅
👉
पोटैशियम ट्राइऑक्सालेटोक्रोमेट(III)
(Potassium tris(oxalato)chromate(III))
व्याख्या (Step by Step) 👉
इस संकुल में:
👉 K3 = 3 पोटैशियम आयन (cation)
👉 संकुल आयन = [Cr(C2O4)3]3−
👉 C2O42− = ऑक्सालेटो (oxalato) ligand
👉 ऐसे 3 ligands हैं, इसलिए tris(oxalato) लिखा जाता है।
Cr की ऑक्सीकरण अवस्था निकालते हैं
मान लें Cr की ऑक्सीकरण अवस्था =
x
👉 x + 3(−2) = −3
👉 x − 6 = −3
👉 x = +3
✅ इसलिए धातु का नाम होगा क्रोमेट(III) or chromate(III) (क्योंकि संकुल आयन anionic है, इसलिए chromium → chromate)
क्या आप जानते हैं? 🤔📌
✅ जब
ligand
का नाम पहले से complex type का हो (जैसे
oxalato),
और संख्या 2 से अधिक हो, तो
di/tri
की जगह अक्सर
bis/tris
इस्तेमाल किया जाता है।
✅ Anionic complex में metal के नाम के अंत में अक्सर “-ate” लगाया जाता है (जैसे chromate, ferrate, cuprate)।
(v)
ग्रीन्यार अभिकर्मक
का कोई एक उदाहरण लिखिए।
Answer ✅
👉
CH3MgBr
(मिथाइल मैग्नीशियम ब्रोमाइड)
व्याख्या (Step by Step) 👉
✅ ग्रीन्यार अभिकर्मक का सामान्य सूत्र होता है:
👉 R–Mg–X
जहाँ,
R = ऐल्किल / ऐरिल समूह
X = Cl, Br, I
इसलिए CH3MgBr एक सही उदाहरण है।
क्या आप जानते हैं? 🤔📌
✅
ग्रीन्यार अभिकर्मक
बहुत
क्रियाशील
होते हैं और
नमी/पानी
से तुरंत अभिक्रिया कर लेते हैं।
✅ इन्हें सामान्यतः शुष्क ईथर (dry ether) में तैयार और उपयोग किया जाता है।
(vi)
फिटिंग अभिक्रिया (Fittig reaction)
का रासायनिक समीकरण लिखिए।
Answer ✅
✅
फिटिंग अभिक्रिया (Fittig reaction)
में
एरिल हैलाइड
की अभिक्रिया
सोडियम (Na)
के साथ
शुष्क ईथर (dry ether)
में कराकर
बाइएरिल (Biaryl)
प्राप्त किया जाता है।
👉 सामान्य समीकरण:
2Ar–X + 2Na ⟶ Ar–Ar + 2NaX (dry ether)
👉 उदाहरण:
2C6H5Cl + 2Na ⟶ C6H5–C6H5 + 2NaCl (dry ether)
(क्लोरोबेंजीन से बाइफिनाइल बनता है)
व्याख्या (Step by Step) 👉
• इसमें
दो एरिल हैलाइड अणु
आपस में जुड़ते हैं।
• Na धातु युग्मन कराती है।
• उत्पाद में Ar–Ar बंध बनता है।
✅ इसलिए इसे युग्मन अभिक्रिया भी माना जाता है।
क्या आप जानते हैं? 🤔📌
✅
Wurtz reaction
में
alkyl halides
जुड़ते हैं, जबकि
Fittig reaction
में
aryl halides
जुड़ते हैं।
✅ Wurtz–Fittig reaction में एक alkyl halide + aryl halide मिलकर alkyl benzene बनाते हैं।
(viii)
निम्नलिखित यौगिकों को
जलीय विलयन
में उनकी
क्षारीय प्रबलता के बढ़ते क्रम
में व्यवस्थित कीजिए।
NH3, C2H5NH2, (C2H5)2NH, (C2H5)3N
NH3, C2H5NH2, (C2H5)2NH, (C2H5)3N
Answer ✅
👉
NH3 < (C2H5)3N < C2H5NH2 < (C2H5)2NH
✅ अर्थात जलीय विलयन में क्षारीय प्रबलता का बढ़ता क्रम यही है।
व्याख्या (Step by Step) 👉
जलीय विलयन में
एमीन्स की क्षारीय प्रबलता
केवल
+I effect
पर नहीं, बल्कि
विलायकन (जलयोजन)
पर भी निर्भर करती है।
1) एल्काइल समूह का +I effect
👉
इथाइल समूह
N पर
इलेक्ट्रॉन घनत्व
बढ़ाता है।
✅ इसलिए amines, NH3 से अधिक क्षारीय होते हैं।
2) लेकिन जलीय विलयन में जलयोजन भी होता है
👉 प्रोटोनीकरण के बाद जो
ion
बनता है, उसे
पानी स्थायी करता है।
👉 द्वितीयक अमाइन का संयुग्मी अम्ल अच्छी तरह स्थायी होता है और पर्याप्त +I effect भी मिलता है।
✅ इसलिए यह सबसे अधिक क्षारीय होता है।
3) Tertiary amine क्यों पीछे रह जाता है?
👉
(C2H5)3N
में
+I effect
तो ज्यादा है,
❌ लेकिन प्रोटोनीकृत आयन का जलयोजन, त्रिविम बाधा के कारण कम हो जाता है।
इसलिए जलीय माध्यम में तृतीयक एमीन, प्राथमिक/द्वितीयक से कम क्षारीय हो जाता है।
✅ इसी कारण क्रम होता है:
👉 2° amine > 1° amine > 3° amine > NH3
क्या आप जानते हैं? 🤔📌
✅
गैस अवस्था
में क्षारीय प्रबलता का क्रम अलग होता है, क्योंकि वहाँ
विलायकन (जलयोजन)
नहीं होता।
✅ जलीय विलयन में amines की क्षारीय प्रबलता समझने के लिए +I effect + hydration effect दोनों देखना जरूरी है।
(ix)
रेशेदार प्रोटीन (Fibrous protein)
के दो उदाहरण लिखिए।
Answer ✅
👉
केराटिन (Keratin)
👉 कोलेजन (Collagen)
व्याख्या (Step by Step) 👉
✅
रेशेदार (Fibrous) प्रोटीन
लंबे, धागेनुमा और सामान्यतः
जल में अघुलनशील
होते हैं।
✅ ये शरीर में संरचनात्मक कार्य करते हैं, जैसे त्वचा, बाल, नाखून, संयोजी ऊतक आदि को मजबूती देना।
केराटिन → बाल, नाखून, त्वचा में पाया जाता है
कोलेजन → संयोजी ऊतकों (connective tissues), त्वचा, टेंडन आदि में पाया जाता है
क्या आप जानते हैं? 🤔📌
✅
फाइब्रोइन (Fibroin)
(रेशम में) भी एक
रेशेदार प्रोटीन
है।
✅ रेशेदार प्रोटीन की तुलना में गोलाकार (globular) प्रोटीन अधिकतर क्रियात्मक (functional) होते हैं, जैसे एंजाइम।
(x)
DNA
की
द्विकुंडली (Double Helix)
संरचना का चित्र बनाइए।
Answer ✅
👉 नीचे DNA की द्विकुंडली संरचना का
सरल रेखाचित्र (diagram)
दिया गया है:
5′ Sugar-Phosphate backbone Sugar-Phosphate backbone 3′
\ /
A ⋯⋯ T
\ /
\ /
G ⋯⋯⋯ C
\ /
\ /
T ⋯⋯ A
\ /
\ /
C ⋯⋯⋯ G
/ \
/ \
A ⋯⋯ T
/ \
/ \
G ⋯⋯⋯ C
/ \
/ \
3′ Sugar-Phosphate backbone Sugar-Phosphate backbone 5′
(Please refer your NCERT book to see diagram)
✅ A = Adenine, T = Thymine, G = Guanine, C = Cytosine
✅ A–T के बीच 2 H-बॉन्ड और G–C के बीच 3 H-बॉन्ड होते हैं।
व्याख्या (Step by Step) 📌
👉 DNA
दो पॉलीन्यूक्लियोटाइड श्रृंखलाओं
से बना होता है।
👉 दोनों श्रृंखलाएँ आपस में कुंडलित (helix) होकर रहती हैं।
👉 बाहर की ओर शर्करा-फॉस्फेट रीढ़ होती है।
👉 अंदर की ओर नाइट्रोजन क्षारक होते हैं जो युग्म बनाते हैं:
👉 A–T और G–C
👉 दोनों strands पूरक (complementary) और विपरीत दिशा (antiparallel) में होती हैं।
क्या आप जानते हैं? 🤔📌
✅ DNA की द्विकुंडली संरचना का मॉडल
Watson और Crick
ने दिया था।
✅ G–C pairing में 3 H-बॉन्ड होने के कारण यह A–T से अधिक मजबूत होती है।
लघुत्तरात्मक प्रश्न: (उत्तर सीमा लगभग 50 शब्द)
(4)
4.0 g NaOH
को जल में घोलकर
500 mL विलयन
बनाया गया। विलयन की
मोलरता
की गणना कीजिए।
Answer ✅
👉 विलयन की मोलरता =
0.20 M ✅
व्याख्या (Step by Step) 👉
Step 1: NaOH के मोलर द्रव्यमान (Molar mass) निकालें
NaOH
=
Na (23)
+
O (16)
+
H (1)
👉 मोलर द्रव्यमान = 40 g mol−1
Step 2: NaOH के मोल (moles) निकालें
सूत्र:
👉 मोल = द्रव्यमान / मोलर द्रव्यमान
👉 मोल = 4.0 / 40
👉 मोल = 0.10 mol
Step 3: आयतन को लीटर में बदलें
500 mL
=
0.500 L
Step 4: मोलरता (Molarity) निकालें
सूत्र:
👉 M = मोल / आयतन (L में)
👉 M = 0.10 / 0.500
👉 M = 0.20 mol L−1
✅ इसलिए, विलयन की मोलरता = 0.20 M
क्या आप जानते हैं? 🤔📌
✅
मोलरता (M)
तापमान पर निर्भर करती है क्योंकि यह
विलयन के आयतन
पर आधारित होती है।
✅ NaOH एक strong base है और पानी में लगभग पूर्णतः आयनीकृत हो जाता है।
(5)
प्रतिलोम परासरण
को दर्शाने वाला चित्र बनाइए।
Answer ✅
👉 नीचे
प्रतिलोम परासरण (Reverse Osmosis, RO)
का सरल चित्र दिया गया है
(refer NCERT book)
┌───────────────────────────┐ ┌───────────────────────────┐
│ अधिक सांद्र विलयन │ │ शुद्ध जल │
│ (salty/impure) │ │ │
│ │ │ │
│ बाहरी दाब P > π │ │ │
│ ───────────────▶ │ │ │
│ │ │ │
└──────────────┬────────────┘ └────────────┬──────────────┘
│ │
│ अर्द्धपारगम्य झिल्ली │
│ ║║║║║║║║║║║║║║ │
│ │
└──────────── जल अणु ───────────▶
व्याख्या (Step by Step) 👉
✅
प्रतिलोम परासरण (RO)
में
अधिक सांद्र (salty/impure) विलयन
पर
परासरण दाब
से अधिक
बाहरी दाब
लगाया जाता है।
👉 तब जल अणु अर्द्धपारगम्य झिल्ली से होकर
अधिक सांद्र विलयन → शुद्ध जल की ओर जाते हैं (जो सामान्य परासरण की विपरीत दिशा है)।
✅ इस प्रक्रिया में:
• जल झिल्ली से गुजर जाता है
• लवण/अशुद्धियाँ पीछे रह जाती हैं
क्या आप जानते हैं? 🤔📌
✅ घरों में इस्तेमाल होने वाले
RO water purifiers
इसी सिद्धांत पर काम करते हैं।
✅ RO झिल्ली बहुत सूक्ष्म होती है, जो कई घुले हुए लवण, धातु आयन और अशुद्धियाँ रोक सकती है।
(6)
निकेल–कैडमियम सेल
का नामांकित चित्र बनाइए।
Answer ✅
👉 नीचे
निकेल–कैडमियम (Ni–Cd) सेल
का सरल नामांकित चित्र दिया गया है:
(Refer NCERT Book)
व्याख्या (Step by Step) 👉
✅
Ni–Cd cell
एक
रिचार्जेबल (rechargeable)
सेल है।
मुख्य भाग
•
धनाग्र (+):
निकेल ऑक्साइड हाइड्रॉक्साइड, NiO(OH)
• ऋणाग्र (−): कैडमियम, Cd
• इलेक्ट्रोलाइट: KOH (पोटैशियम हाइड्रॉक्साइड) विलयन
• Separator: इलेक्ट्रोड को अलग रखता है ताकि short circuit न हो
कार्य सिद्धांत (Discharge के समय)
•
कैडमियम इलेक्ट्रोड
पर
oxidation
होता है
• निकेल इलेक्ट्रोड पर reduction होता है
• इलेक्ट्रॉन बाह्य परिपथ में Cd → Ni की ओर जाते हैं
क्या आप जानते हैं? 🤔📌
✅
Ni–Cd सेल
को कई बार
recharge
किया जा सकता है, इसलिए इसे
secondary cell
कहते हैं।
✅ पुराने rechargeable उपकरणों (जैसे emergency lights, cordless devices) में Ni–Cd cell बहुत उपयोग होता था।
(7)
Fe2+(aq.)
आयन के लिए
प्रचक्रण-केवल (spin-only) चुंबकीय आघूर्ण
की गणना कीजिए।
Answer ✅
👉
Fe2+(aq.)
के लिए प्रचक्रण-भ्राम्य चुंबकीय आघूर्ण
μ = 4.90 BM (लगभग) ✅
व्याख्या (Step by Step) 👉
Step 1: Fe का इलेक्ट्रॉनिक विन्यास लिखें
Fe (Z = 26):
👉 [Ar] 3d6 4s2
Fe2+ बनने पर 2 electron निकलते हैं (पहले 4s से):
👉 Fe2+ = [Ar] 3d6
Step 2: Aqueous Fe2+ में अयुग्मित इलेक्ट्रॉन
H2O
एक
weak field ligand
है, इसलिए
Fe2+(aq.)
सामान्यतः
high spin d6
होता है।
✅ उच्च चक्रण d6 में 4 अयुग्मित इलेक्ट्रॉन होते हैं।
👉 n = 4
Step 3: प्रचक्रण-भ्राम्य चुंबकीय आघूर्ण का सूत्र लगाएँ
सूत्र:
👉 μ = √[n(n+2)] BM
अब n = 4 रखने पर:
👉 μ = √[4(4+2)]
👉 μ = √(4×6)
👉 μ = √24
अब √24 का मान:
• 4×4 = 16
• 5×5 = 25
तो √24 ≈ 4.90
✅ इसलिए,
👉 μ = 4.90 BM (Bohr Magneton)
क्या आप जानते हैं? 🤔📌
✅ यदि ligand
strong field
हो, तो
d-electrons pairing
बढ़ सकती है और चुंबकीय
आघूर्ण कम होता है।
✅ Aqueous Fe2+ (जैसे [Fe(H2O)6]2+) सामान्यतः अनुचुंबकीय
होता है क्योंकि इसमें अयुग्मित इलेक्ट्रॉन होते हैं।
(8)
लैन्थेनॉइड संकुचन
को समझाइए।
Answer ✅
✅
लैन्थेनॉइड संकुचन (Lanthanoid Contraction)
वह घटना है जिसमें
La से Lu तक
जाते समय
परमाण्विक तथा आयनिक त्रिज्या
धीरे-धीरे घटती जाती है, जबकि
परमाणु क्रमांक
बढ़ता रहता है।
व्याख्या (Step by Step) 👉
1) यह क्यों होता है?
लैन्थेनॉइड श्रेणी में इलेक्ट्रॉन क्रमशः
4f-कक्षाओं
में भरते हैं।
✅ 4f-इलेक्ट्रॉनों की shielding (परिरक्षण) क्षमता बहुत कमजोर होती है।
इस कारण नाभिक का आकर्षण बाहरी इलेक्ट्रॉनों पर अधिक प्रभावी हो जाता है।
👉 परिणाम: इलेक्ट्रॉन नाभिक की ओर अधिक खिंचते हैं
✅ इसलिए आकार (radius) कम होता जाता है।
2) सरल भाषा में समझें
प्रोटॉन (नाभिकीय आवेश)
बढ़ रहे हैं
लेकिन 4f इलेक्ट्रॉन उस बढ़े हुए आकर्षण को अच्छी तरह shield नहीं कर पाते
इसलिए effective nuclear charge बढ़ता है
✅ और त्रिज्या घटती जाती है
3) इसके महत्वपूर्ण परिणाम
✅ (i)
4d और 5d श्रेणी
के तत्वों के आकार लगभग समान हो जाते हैं
उदाहरण: Zr और Hf की त्रिज्याएँ बहुत मिलती-जुलती हैं।
✅ (ii) लैन्थेनॉइड्स के रासायनिक गुण बहुत समान होते हैं
इसलिए इन्हें अलग करना कठिन होता है।
✅ (iii) बेसिक शक्ति में परिवर्तन
लैन्थेनॉइड हाइड्रॉक्साइड्स की basicity सामान्यतः श्रेणी में आगे बढ़ने पर घटती है।
क्या आप जानते हैं? 🤔📌
✅
लैन्थेनॉइड संकुचन
का प्रभाव केवल
लैन्थेनॉइड्स
तक सीमित नहीं रहता, यह बाद के कई तत्वों
(विशेषकर 5d तत्वों)
के गुणों को भी प्रभावित करता है।
✅ यही कारण है कि Zr और Hf जैसे तत्व रासायनिक रूप से बहुत समान व्यवहार दिखाते हैं।
(9)
निम्नलिखित पदों को परिभाषित कीजिए —
(अ) ध्रुवण घूर्णकता
(ब) काइरालता
(अ) ध्रुवण घूर्णकता
(ब) काइरालता
Answer ✅
(अ) ध्रुवण घूर्णकता (Optical Rotation / विशिष्ट घूर्णन से संबंधित गुण)
✅ किसी प्रकाशीय सक्रिय (optically active) पदार्थ द्वारा समतल ध्रुवित प्रकाश (plane polarised light) के कम्पन तल को एक निश्चित कोण से घुमा देने के गुण को ध्रुवण घूर्णकता कहते हैं।
👉 यदि घूर्णन दाईं ओर हो तो दक्षिणावर्त / dextrorotatory (+)
👉 यदि घूर्णन बाईं ओर हो तो वामावर्त / laevorotatory (−)
(ब) काइरालता (Chirality)
✅ किसी अणु का वह गुण, जिसके कारण उसका दर्पण प्रतिबिंब (mirror image) उस अणु पर अध्यारोपित (superimpose) नहीं किया जा सकता, काइरालता कहलाता है।
👉 ऐसे अणु को काइरल (chiral) कहते हैं।
व्याख्या (Step by Step) 👉
(अ) ध्रुवण घूर्णकता
• सामान्य प्रकाश कई तल में कम्पन करता है।
• जब इसे polarizer से गुजारते हैं, तो समतल ध्रुवित प्रकाश मिलता है।
• यदि यह प्रकाश किसी प्रकाशीय सक्रिय (optically active) पदार्थ (जैसे glucose solution) से गुजरे, तो उसका तल घूम जाता है।
✅ यही घटना ध्रुवण घूर्णन कहलाती है।
(ब) काइरालता
• काइरालता प्रायः तब होती है जब किसी कार्बन से
चार अलग-अलग समूह
जुड़े हों।
✅ ऐसे कार्बन को असममित कार्बन (chiral carbon) कहते हैं।
• ऐसे यौगिकों के दो दर्पण-प्रतिबिंब रूप बनते हैं, जिन्हें एनेन्टियोमर (enantiomers) कहते हैं।
क्या आप जानते हैं? 🤔📌
✅ हर काइरल यौगिक में सामान्यतः
optical activity
पाई जाती है, लेकिन
racemic mixture
प्रकाश को नहीं घुमाता।
✅ काइरालता जैविक रसायन (Biochemistry) और दवाइयों (Pharmaceuticals) में बहुत महत्वपूर्ण है, क्योंकि दो enantiomers का प्रभाव अलग-अलग हो सकता है।
(10)
एकाण्विक नाभिकस्नेही प्रतिस्थापन अभिक्रिया (SN1)
की क्रियाविधि को समझाइए।
Answer ✅
✅
SN1 (Unimolecular Nucleophilic Substitution)
अभिक्रिया वह प्रतिस्थापन अभिक्रिया है जिसमें
वेग-निर्धारक चरण (rate determining step)
में केवल
एक अणु (substrate)
भाग लेता है।
👉 यह अभिक्रिया दो चरणों में होती है और बीच में कार्बोकैटायन (carbocation) बनता है।
व्याख्या (Step by Step) 👉
सामान्य अभिक्रिया
👉
R–X + Nu− → R–Nu + X−
जहाँ
• R–X = alkyl halide (substrate)
• Nu− = nucleophile
• X− = leaving group
Step 1: कार्बोकैटायन का निर्माण (धीमा चरण / RDS)
👉
R–X ⟶ R+ + X− (slow)
✅ यह सबसे धीमा चरण है, इसलिए अभिक्रिया की दर इसी पर निर्भर करती है।
✅ इसी कारण इसे SN1 कहते हैं (unimolecular in rate-determining step).
Rate law:
👉 Rate = k[R–X]
Step 2: न्यूक्लियोफाइल का आक्रमण (तेज़ चरण)
👉
R+ + Nu− ⟶ R–Nu (fast)
✅ बना हुआ कार्बोकैटायन समतलीय (planar) होता है, इसलिए न्यूक्लियोफाइल दोनों ओर से attack कर सकता है।
यदि न्यूक्लियोफाइल उदासीन हो (जैसे H2O)
पहले
प्रोटोनेटेड उत्पाद
बनता है, फिर
H+
निकल जाता है।
👉 R+ + H2O ⟶ R–OH2+
👉 R–OH2+ ⟶ R–OH + H+
SN1 की मुख्य विशेषताएँ
✅
तृतीयक (3°) alkyl halides
में अधिक अनुकूल
(stable carbocation)
✅ ध्रुवीय प्रोटिक विलायक (polar protic solvents) में तेज
✅ रेसेमिकरण हो सकती है (यदि chiral center हो) क्योंकि कार्बोकैटायन समतलीय होता है
✅ पुनर्विन्यास (hydride shift / methyl shift) संभव है
क्या आप जानते हैं? 🤔📌
✅
SN1
और
E1
अभिक्रियाएँ अक्सर साथ-साथ हो सकती हैं क्योंकि दोनों में
कार्बोकैटायन मध्यवर्ती
बनता है।
✅ कार्बोकैटायन के स्थायीत्व का क्र: 3° > 2° > 1° > CH3+, इसलिए SN1 सामान्यतः 3° substrates में सबसे आसान होती है।
(11)
निम्नलिखित यौगिकों के संरचनात्मक सूत्र लिखिए —
(अ) आइसोप्रोपिल ऐल्कोहॉल
(ब) द्वितीयक-ब्यूटिल ऐल्कोहॉल
(अ) आइसोप्रोपिल ऐल्कोहॉल
(ब) द्वितीयक-ब्यूटिल ऐल्कोहॉल
Answer ✅
(अ) आइसोप्रोपिल ऐल्कोहॉल (Isopropyl alcohol)
👉 संरचनात्मक सूत्र:
CH3–CH(OH)–CH3
✅ IUPAC नाम: Propan-2-ol
(ब) द्वितीयक-ब्यूटिल ऐल्कोहॉल (sec-Butyl alcohol)
👉 संरचनात्मक सूत्र:
CH3–CH(OH)–CH2–CH3
✅ IUPAC नाम: Butan-2-ol
व्याख्या (Step by Step) 👉
👉 आइसोप्रोपिल एल्कोहोल में
3 कार्बन श्रृंखला
होती है और
–OH
बीच वाले कार्बन पर होता है →
propan-2-ol
👉 द्वितीयक-ब्यूटिल ऐल्कोहॉल में 4- कार्बन श्रृंखला होती है और –OH दूसरे कार्बन पर होता है → butan-2-ol
✅ दोनों ही द्वितीयक ऐल्कोहॉल हैं क्योंकि –OH वाला कार्बन दो अन्य कार्बन से जुड़ा है।
क्या आप जानते हैं? 🤔📌
✅
Isopropyl alcohol
का उपयोग
sanitizer/rubbing alcohol
के रूप में किया जाता है।
✅ Common names (जैसे iso-, sec-) practical use में बहुत मिलते हैं, लेकिन exams में IUPAC नाम लिखना बेहतर रहता
(12)
फीनॉल की अनुनादी संरचनाएँ बनाइए।
Answer ✅
✅
फीनॉल (C6H5OH)
में ऑक्सीजन के
lone pair
के कारण बेंजीन वलय में
+M प्रभाव (resonance donation)
होता है।
इससे ऑर्थो (o) और पैरा (p) स्थानों पर इलेक्ट्रॉन घनत्व बढ़ता है।
👉 फीनॉल की मुख्य अनुनादी संरचनाएँ (canonical forms) नीचे दी जा रही हैं:
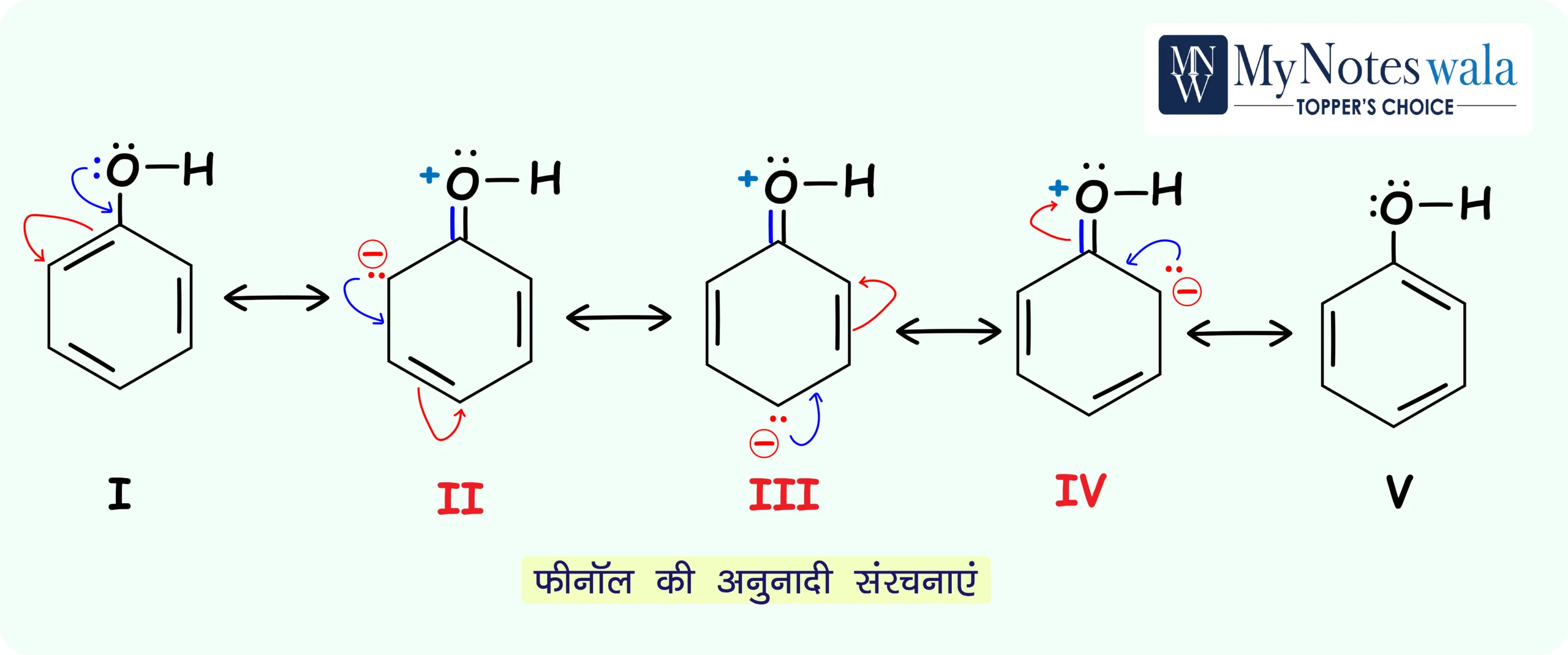
अर्थात resonance के कारण ring के दोनों ortho और एक para स्थान पर ऋण आवेश का आंशिक वितरण माना जाता है।
व्याख्या (Step by Step) 👉
कैसे resonance होता है?
• O-atom पर
lone pair
होता है।
• यह lone pair बेंजीन रिंग में चला जाता है।
• परिणामस्वरूप:
o O पर आंशिक धन आवेश (δ+)
o O and P positions पर आंशिक ऋण आवेश (δ−) आ जाता है।
✅ इसी कारण फीनॉल electrophilic substitution के लिए activated होता है और ortho/para directing होता है।
इसी कारण से फीनॉल इलेक्ट्रोफिलिक प्रतिस्थापन सक्रिय होता है और ऑर्थो/पैरा निर्दिष्टकारी होता है।
क्या आप जानते हैं? 🤔📌
✅ फीनॉल का
–OH group,
halobenzene के
–X group
की तुलना में ring को बहुत अधिक activate करता है क्योंकि oxygen का
resonance donation
stronger होता है।
✅ यही कारण है कि फीनॉल bromine water से आसानी से 2,4,6-tribromophenol देता है।
(13)
निम्नलिखित रासायनिक समीकरणों को पूर्ण कीजिए एवं मुख्य उत्पाद लिखिए —
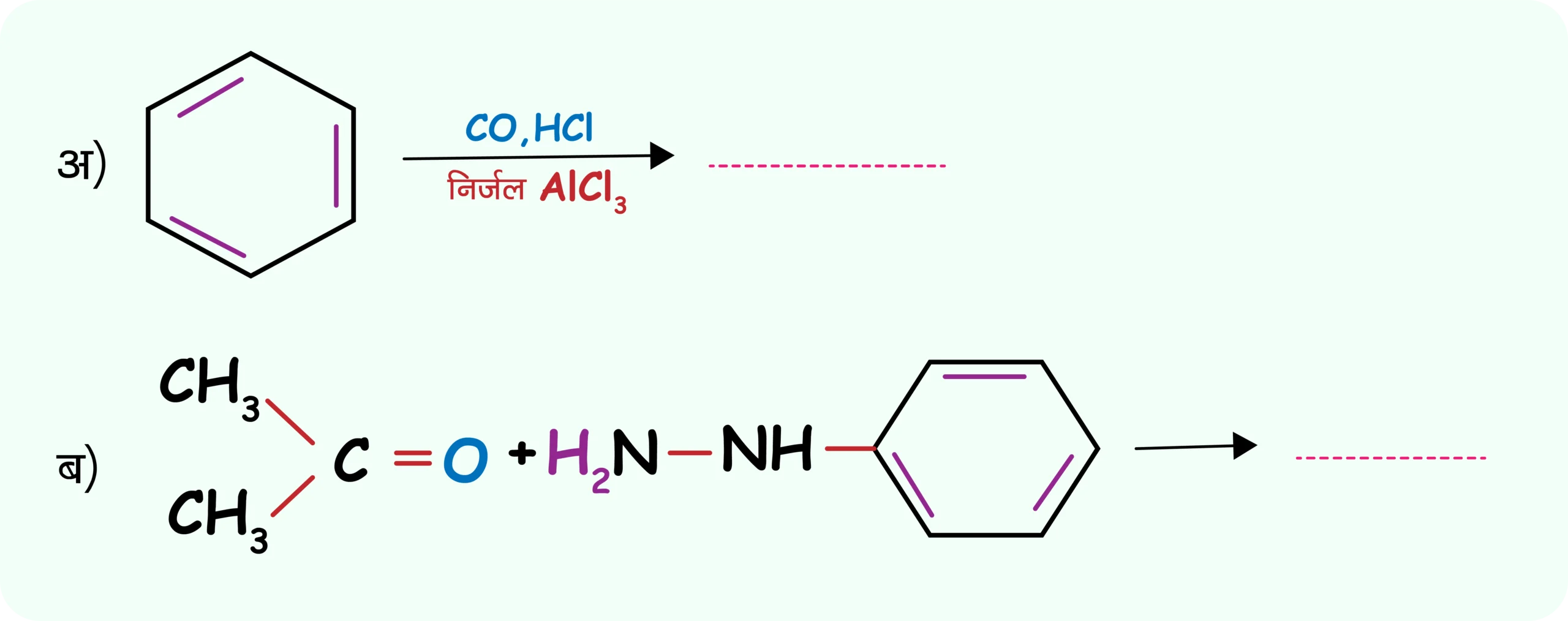

Answer ✅
(अ) बेंजीन + CO, HCl / निर्जल AlCl3 → ?
👉 मुख्य उत्पाद: बेंजैल्डिहाइड (Benzaldehyde), C6H5CHO
(यह Gattermann–Koch formylation reaction है)
(ब) एसीटोन + फिनाइलहाइड्राजीन → ?
👉 मुख्य उत्पाद: एसीटोन फिनाइलहाइड्राजोन (Acetone phenylhydrazone)
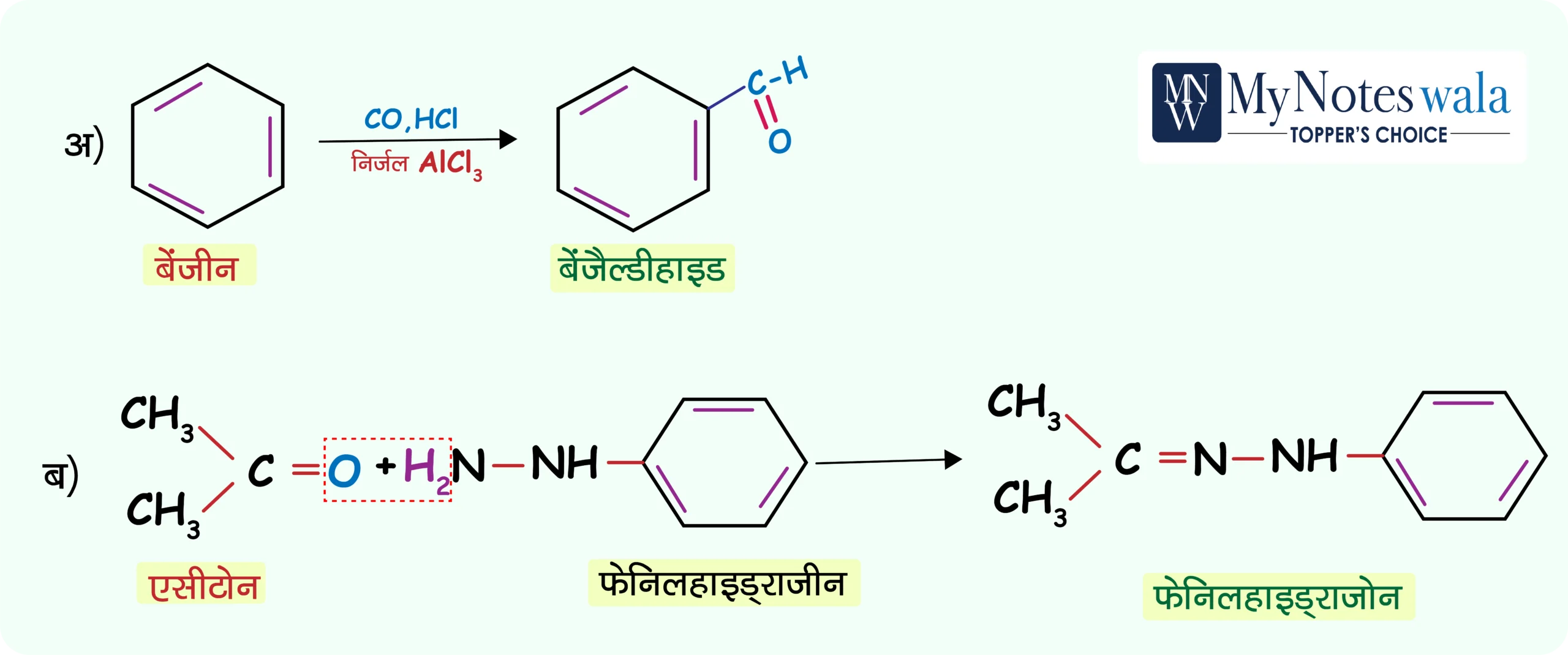
व्याख्या (Step by Step) 👉
(अ) पहली अभिक्रिया
•
Benzene ring
पर
–CHO (formyl group)
जुड़ता है।
• Reagents CO + HCl तथा AlCl3/CuCl की उपस्थिति में aromatic ring का formylation होता है।
✅ इसलिए product = benzaldehyde
(ब) दूसरी अभिक्रिया
•
Ketone (acetone)
का carbonyl group
(C=O)
phenylhydrazine से अभिक्रिया करता है।
• यह condensation reaction है, जिसमें H2O निकलता है।
✅ Product में C=N–NHPh group बनता है, जिसे phenylhydrazone कहते हैं।
क्या आप जानते हैं? 🤔📌
✅
Aldehydes/ketones
की पहचान के लिए
hydrazone derivatives
बनाना एक important method है।
✅ Gattermann–Koch reaction aromatic compounds में –CHO group introduce करने की classic reaction है।
(14)
(अ) फैराडे का विद्युतअपघटन का प्रथम नियम
लिखिए।
(ब) 298 K पर 0.01 M KCl विलयन की चालकता 0.00141 S cm−1 है। 0.01 M KCl विलयन की मोलर चालकता की गणना कीजिए।
(ब) 298 K पर 0.01 M KCl विलयन की चालकता 0.00141 S cm−1 है। 0.01 M KCl विलयन की मोलर चालकता की गणना कीजिए।
Answer ✅
(अ) फैराडे का विद्युतअपघटन का प्रथम नियम
✅ विद्युतअपघटन के दौरान इलेक्ट्रोड पर निक्षेपित (या मुक्त) पदार्थ की मात्रा, विलयन में प्रवाहित कुल विद्युत आवेश (Q) के समानुपाती होती है।
👉 गणितीय रूप:
m ∝ Q
या
m = ZIt
जहाँ,
m = निक्षेपित पदार्थ का द्रव्यमान
Z = वैद्युत-रासायनिक तुल्यांक
I = धारा (current)
t = समय
(ब) मोलर चालकता (Molar Conductivity)
✅ मोलर चालकता, Λm = 141 S cm2 mol−1
व्याख्या (Step by Step) 👉
(अ) प्रथम नियम की सरल व्याख्या
यदि अधिक समय तक या अधिक धारा से विद्युत प्रवाहित करेंगे, तो इलेक्ट्रोड पर अधिक पदार्थ जमा होगा।
✅ यानी निकला/जमा पदार्थ ∝ कुल आवेश (I × t)
(ब) मोलर चालकता की गणना
दिया है:
चालकता, κ = 0.00141 S cm−1
सांद्रता, C = 0.01 mol L−1
सूत्र:
👉 Λm = (κ × 1000) / C
मान रखने पर:
👉 Λm = (0.00141 × 1000) / 0.01
👉 Λm = 1.41 / 0.01
👉 Λm = 141 S cm2 mol−1
✅ अतः 0.01 M KCl विलयन की मोलर चालकता = 141 S cm2 mol−1
क्या आप जानते हैं? 🤔📌
✅ मोलर चालकता
dilution (सांद्रता घटने)
पर सामान्यतः बढ़ती है।
✅ KCl solution का उपयोग conductivity cell की cell constant calibration में भी किया जाता है।
अथवा
(अ) फैराडे का विद्युतअपघटन का द्वितीय नियम
लिखिए।
(ब) 298 K पर 0.05 M NaOH विलयन की चालकता 0.01150 S cm−1 है। 0.05 M NaOH विलयन की मोलर चालकता की गणना कीजिए।
(ब) 298 K पर 0.05 M NaOH विलयन की चालकता 0.01150 S cm−1 है। 0.05 M NaOH विलयन की मोलर चालकता की गणना कीजिए।
Answer ✅
(अ) फैराडे का विद्युतअपघटन का द्वितीय नियम
✅ जब समान विद्युत आवेश (same quantity of electricity) विभिन्न विद्युतअपघट्यों से प्रवाहित किया जाता है, तो इलेक्ट्रोड पर निक्षेपित पदार्थों के द्रव्यमान उनके रासायनिक तुल्यांकों (equivalent masses) के समानुपाती होते हैं।
👉 गणितीय रूप:
m1/m2 = E1/E2
जहाँ,
• m1, m2 = निक्षेपित पदार्थों के द्रव्यमान
• E1, E2 = उनके रासायनिक तुल्यांक
(ब) मोलर चालकता (Molar Conductivity)
✅ मोलर चालकता, Λm = 230 S cm2 mol−1
व्याख्या (Step by Step) 👉
(अ) द्वितीय नियम की सरल व्याख्या
यदि अलग-अलग इलेक्ट्रोलाइट्स में एक ही मात्रा की बिजली प्रवाहित की जाए, तो जो पदार्थ इलेक्ट्रोड पर जमा होंगे, उनकी मात्रा उनके
equivalent mass
पर निर्भर करेगी।
✅ यानी:
👉 ज्यादा equivalent mass → ज्यादा द्रव्यमान निक्षेपित
(ब) मोलर चालकता की गणना
दिया है:
• चालकता, κ = 0.01150 S cm−1
• सांद्रता, C = 0.05 mol L−1
सूत्र:
👉 Λm = (κ × 1000) / C
मान रखने पर:
👉 Λm = (0.01150 × 1000) / 0.05
👉 Λm = 11.50 / 0.05
अब भाग दें:
• 11.50 ÷ 0.05 = 230
👉 Λm = 230 S cm2 mol−1
✅ अतः 0.05 M NaOH विलयन की मोलर चालकता = 230 S cm2 mol−1
क्या आप जानते हैं? 🤔📌
✅
NaOH
एक
प्रबल विद्युतअपघट्य (strong electrolyte)
है, इसलिए इसका विलयन अच्छी चालकता दिखाता है।
✅ OH− आयन की गतिशीलता (mobility) बहुत अधिक होती है, इसलिए NaOH की मोलर चालकता अपेक्षाकृत अधिक मिलती है।
(15)
संयोजकता आबंध सिद्धान्त (VBT)
के आधार पर
[FeF6]3−
संकुल आयन की
ज्यामिति
और
चुंबकीय प्रकृति
समझाइए।
Answer ✅
✅
[FeF6]3−
की ज्यामिति
अष्टफलकाकार (Octahedral)
होती है।
✅ यह संकुल बाह्य कक्षक संकुल (outer orbital complex) है।
✅ इसकी चुंबकीय प्रकृति अनुचुंबकीय (paramagnetic) होती है और इसमें 5 अयुग्मित इलेक्ट्रॉन होते हैं।
व्याख्या (Step by Step) 👉
Step 1: Fe की ऑक्सीकरण अवस्था निकालें
संकुल:
[FeF6]3−
मान लें Fe की oxidation state = x
👉 x + 6(−1) = −3
👉 x − 6 = −3
👉 x = +3
✅ अतः धातु आयन = Fe3+
Step 2: Fe3+ का इलेक्ट्रॉनिक विन्यास
Fe (Z = 26) का विन्यास:
👉 [Ar] 3d6 4s2
Fe3+ के लिए 3 इलेक्ट्रॉन निकलेंगे (पहले 4s, फिर 3d):
👉 Fe3+ = [Ar] 3d5
✅ यानी d5 विन्यास
Step 3: लिगैंड की प्रकृति (F−)
✅
F−
एक
दूर्बल क्षेत्र लिगैंड
है।
इसलिए यह इलेक्ट्रॉन को युग्मन नहीं कराता।
👉 d-orbitals में युग्मन नहीं होती, इसलिए Fe3+ उच्च चक्रण रहता है।
Step 4: Hybridisation और Geometry (VBT के अनुसार)
अष्टफलकीय संकुल में 6 लिगैंड जुड़ते हैं, इसलिए
6 सकंरित कक्षक
चाहिए।
क्योंकि F− दूर्बल लिगैंड है, आंतरिक d- कक्षक का युग्मन नहीं होगा।
इसलिए संकरण होता है:
👉 sp3d2 (outer orbital complex)
✅ इससे geometry मिलती है: Octahedral (अष्टफलकाकार)
Step 5: चुंबकीय प्रकृति
Fe3+ = 3d5 (high spin)
✅ इसमें 5 unpaired electrons होते हैं।
इसलिए:
👉 संकुल paramagnetic (अनुचुंबकीय) है।
(यदि spin-only moment पूछें तो)
👉 μ = √[n(n+2)] BM = √[5(5+2)] = √35 ≈ 5.92 BM
क्या आप जानते हैं? 🤔📌
✅
[FeF6]3−
और
[Fe(CN)6]3−
में बड़ा अंतर
ligand strength
की वजह से आता है:
• F− (weak field) → high spin
• CN− (strong field) → low spin
✅ इसी ligand effect के कारण एक ही metal ion के complexes की magnetic nature अलग हो सकती है।
अथवा
प्रश्न
संयोजकता आबंध सिद्धान्त (VBT)
के आधार पर
[Ni(CN)4]2−
संकुल आयन की
ज्यामिति
और
चुंबकीय प्रकृति
समझाइए।
Answer ✅
✅
[Ni(CN)4]2−
की ज्यामिति
समतलीय वर्गाकार (Square planar)
होती है।
✅ यह आंतरिक कक्षक संकुल (inner orbital complex) है।
✅ इसकी चुंबकीय प्रकृति प्रतिचुंबकीय (diamagnetic) होती है (कोई अयुग्मित इलेक्ट्रॉन नहीं)।
व्याख्या (Step by Step) 👉
Step 1: Ni की oxidation state निकालें
संकुल:
[Ni(CN)4]2−
मान लें Ni की oxidation state = x
CN− = −1 (4 ligand)
👉 x + 4(−1) = −2
👉 x − 4 = −2
👉 x = +2
✅ अतः धातु आयन = Ni2+
Step 2: Ni2+ का electronic configuration
Ni (Z = 28):
👉 [Ar] 3d8 4s2
Ni2+ बनने पर 2 electron निकलते हैं (4s से):
👉 Ni2+ = [Ar] 3d8
Step 3: Ligand CN− की प्रकृति
✅
CN−
एक
strong field ligand
है।
यह d-electrons की pairing कराता है।
✅ इसलिए electrons pair होकर inner orbital available कराते हैं।
Step 4: Hybridisation और Geometry (VBT)
चार ligands के लिए
4 hybrid orbitals
चाहिए।
Strong field ligand होने के कारण hybridisation होती है:
👉 dsp2
✅ dsp2 hybridisation से geometry मिलती है:
👉 Square planar (समतलीय वर्गाकार)
Step 5: चुंबकीय प्रकृति
Ni2+ (3d8) में
CN−
ligand pairing करा देता है।
✅ सभी electrons paired हो जाते हैं।
👉 इसलिए complex diamagnetic (प्रतिचुंबकीय) होता है।
क्या आप जानते हैं? 🤔📌
✅
[NiCl4]2−
(weak field ligand
Cl−)
सामान्यतः
tetrahedral
और
paramagnetic
होता है,
जबकि [Ni(CN)4]2− (strong field ligand CN−) square planar और diamagnetic होता है।
✅ यही coordination chemistry का सबसे interesting part है: same metal, different ligands → different geometry + magnetism.
(16)
निम्नलिखित को एक पद में परिवर्तित कीजिए
(केवल रासायनिक समीकरण लिखिए)
—
(अ) बेंजीनडायजोोनियम क्लोराइड से फिनॉल
(ब) ऐनिलीन से 2,4,6-ट्राइब्रोमोऐनिलीन
(स) एथेनामाइड से मेथेनैमीन
(अ) बेंजीनडायजोोनियम क्लोराइड से फिनॉल
(ब) ऐनिलीन से 2,4,6-ट्राइब्रोमोऐनिलीन
(स) एथेनामाइड से मेथेनैमीन
Answer ✅ (केवल समीकरण)
(अ) बेंजीनडायजोोनियम क्लोराइड → फिनॉल
👉 C6H5N2+Cl− + H2O \xrightarrow{\Delta} C6H5OH + N2↑ + HCl
(ब) ऐनिलीन → 2,4,6-ट्राइब्रोमोऐनिलीन
👉 C6H5NH2 + 3Br2(aq) → 2,4,6-C6H2Br3NH2 + 3HBr
(ब्रोमीन जल / bromine water)
(स) एथेनामाइड → मेथेनैमीन (मिथाइलऐमीन)
👉 CH3CONH2 + Br2 + 4NaOH → CH3NH2 + 2NaBr + Na2CO3 + 2H2O
✅ यह हॉफमैन ब्रोमामाइड अभिक्रिया (Hofmann bromamide reaction) है।
व्याख्या (Step by Step) 👉
(अ)
डायजोोनियम लवण का
हाइड्रोलाइसिस
करने पर
फिनॉल
बनता है।
(ब) ऐनिलीन एक strong activating group है, इसलिए bromine water से सीधे 2,4,6-tribromoaniline देता है।
(स) अमाइड का Hofmann degradation करने पर एक कार्बन कम वाला प्राथमिक अमीन बनता है।
क्या आप जानते हैं? 🤔📌
✅
Hofmann bromamide reaction
में product amine में
carbon atoms की संख्या 1 कम
हो जाती है।
✅ Aniline + bromine water reaction में सफेद अवक्षेप (white precipitate) of 2,4,6-tribromoaniline बनता है।
अथवा
प्रश्न
निम्नलिखित को एक पद में परिवर्तित कीजिए
(केवल रासायनिक समीकरण लिखिए)
—
(अ) बेंजीनडायजोोनियम क्लोराइड से सायनोबेंजीन
(ब) ऐनिलीन से बेंजीनडायजोोनियम क्लोराइड
(स) नाइट्रोमेथेन से मेथेनैमीन
(अ) बेंजीनडायजोोनियम क्लोराइड से सायनोबेंजीन
(ब) ऐनिलीन से बेंजीनडायजोोनियम क्लोराइड
(स) नाइट्रोमेथेन से मेथेनैमीन
Answer ✅ (केवल समीकरण)
(अ) बेंजीनडायजोोनियम क्लोराइड → सायनोबेंजीन
👉 C6H5N2+Cl− \xrightarrow{CuCN/KCN} C6H5CN + N2↑ + KCl
✅ (Sandmeyer reaction)
(ब) ऐनिलीन → बेंजीनडायजोोनियम क्लोराइड
👉 C6H5NH2 + NaNO2 + 2HCl \xrightarrow{273-278,K} C6H5N2+Cl− + NaCl + 2H2O
(स) नाइट्रोमेथेन → मेथेनैमीन
👉 CH3NO2 + 3H2 \xrightarrow{Ni} CH3NH2 + 2H2O
(या अपचयन द्वारा: Sn/HCl, Fe/HCl आदि)
व्याख्या (Step by Step) 👉
(अ)
डायजोोनियम समूह को
–CN
से replace किया जाता है
(Sandmeyer type conversion)।
(ब) ऐनिलीन का diazotisation NaNO2 + HCl से 273–278 K पर किया जाता है।
(स) नाइट्रो यौगिक का reduction करने पर प्राथमिक अमीन बनता है।
क्या आप जानते हैं? 🤔📌
✅
बेंजीनडायजोोनियम लवण
aromatic compounds के कई conversions में बहुत
useful intermediate
होता है।
✅ Diazonium salts को सामान्यतः निम्न ताप (0–5°C) पर स्थिर रखा जाता है।
निबंधात्मक प्रश्न - उत्तर सीमा लगभग 250 शब्द
(17)
(अ) अभिक्रिया की आणविकता
को परिभाषित कीजिए।
(ब) शून्य कोटि अभिक्रिया के लिए अर्धायु का व्यंजक व्युत्पन्न कीजिए।
(स) दर्शाइए कि एक प्रथम कोटि अभिक्रिया में 99.9% अभिक्रिया पूर्ण होने में लगा समय अर्धायु का 10 गुना होता है। (दिया है log1010 = 1)
(ब) शून्य कोटि अभिक्रिया के लिए अर्धायु का व्यंजक व्युत्पन्न कीजिए।
(स) दर्शाइए कि एक प्रथम कोटि अभिक्रिया में 99.9% अभिक्रिया पूर्ण होने में लगा समय अर्धायु का 10 गुना होता है। (दिया है log1010 = 1)
Answer ✅
(अ) अभिक्रिया की आणविकता (Molecularity)
✅ किसी प्राथमिक (elementary) अभिक्रिया में एक साथ टकराने वाले अभिकारक कणों (atoms/ions/molecules) की संख्या को आणविकता कहते हैं।
👉 यह हमेशा पूर्णांक (1, 2, 3...) होती है।
👉 जैसे: एकअणुक, द्विअणुक, त्रिअणुक |
(ब) शून्य कोटि अभिक्रिया के लिए अर्धायु
✅ शून्य कोटि अभिक्रिया के लिए अर्धायु (t1/2) का व्यंजक:
👉 t1/2 = [A]0 / 2k
(स) प्रथम कोटि अभिक्रिया में 99.9% पूर्ण होने का समय
✅ सिद्ध होता है कि:
👉 t99.9% = 10 t1/2
व्याख्या (Step by Step) 👉
(अ) आणविकता की व्याख्या
• यह केवल
प्राथमिक अभिक्रिया
के लिए परिभाषित की जाती है।
• पूरी जटिल अभिक्रिया की आणविकता सामान्यतः नहीं दी जाती।
✅ उदाहरण:
👉 NO + O3 → NO2 + O2 (bimolecular)
(ब) शून्य कोटि अभिक्रिया के अर्धायु का व्युत्पन्न
शून्य कोटि के लिए integrated rate equation:
👉 [A]t = [A]0 − kt
अर्धायु पर,
👉 [A]t = [A]0/2
तो समीकरण में रखें:
👉 [A]0/2 = [A]0 − kt1/2
अब rearrange करें:
👉 kt1/2 = [A]0 − [A]0/2
👉 kt1/2 = [A]0/2
अतः,
👉 t1/2 = [A]0 / 2k
✅ इससे स्पष्ट है कि शून्य-कोटि अभिक्रिया में अर्ध-आयु, प्रारंभिक सांन्द्रता पर निर्भर करता है।
(स) सिद्ध कीजिए: प्रथम कोटि अभिक्रिया में 99.9% पूर्ण होने का समय = 10 × अर्धायु
Step 1: First-order equation
👉
t = (2.303/k) log([A]0/[A]t)
Step 2: 99.9% completion पर
99.9% अभिक्रिया पूर्ण ⇒ 0.1% क्रियाकारक बचा |
👉 शेष अंश = 0.1/100 = 0.001 = 10−3
अर्थात
👉 [A]t = 0.001 [A]0
तो,
👉 [A]0/[A]t = 1000 = 103
अब first-order equation में रखें:
👉 t99.9% = (2.303/k) log(103)
👉 t99.9% = (2.303/k) × 3 (क्योंकि log1010 = 1)
👉 t99.9% = 6.909/k
Step 3: First-order half-life
👉
t1/2 = 0.693/k
अब अनुपात लें:
👉 t99.9% / t1/2 = (6.909/k) / (0.693/k)
👉 t99.9% / t1/2 = 9.97 ≈ 10
✅ अतः सिद्ध हुआ:
👉 t99.9% ≈ 10 t1/2
क्या आप जानते हैं? 🤔📌
✅
First-order reaction
की half-life
initial concentration से independent
होती है।
✅ जबकि zero-order reaction की half-life initial concentration पर depend करती है।
अथवा
प्रश्न
(अ) संघट्ट आवृत्ति
को परिभाषित कीजिए।
(ब) प्रथम कोटि अभिक्रिया के लिए अर्धायु का व्यंजक व्युत्पन्न कीजिए।
(स) दर्शाइए कि एक प्रथम कोटि अभिक्रिया में 75% अभिक्रिया पूर्ण होने में लगा समय अर्धायु का दुगुना होता है।
(दिया है: log102 = 0.3010, log1010 = 1)
(ब) प्रथम कोटि अभिक्रिया के लिए अर्धायु का व्यंजक व्युत्पन्न कीजिए।
(स) दर्शाइए कि एक प्रथम कोटि अभिक्रिया में 75% अभिक्रिया पूर्ण होने में लगा समय अर्धायु का दुगुना होता है।
(दिया है: log102 = 0.3010, log1010 = 1)
Answer ✅
(अ) संघट्ट आवृत्ति (Collision Frequency)
✅ गैसीय अभिक्रिया में प्रति इकाई समय और प्रति इकाई आयतन में अभिकारक कणों के बीच होने वाले कुल संघट्टों (collisions) की संख्या को संघट्ट आवृत्ति कहते हैं।
(ब) प्रथम कोटि अभिक्रिया के लिए अर्धायु
✅ प्रथम कोटि अभिक्रिया के लिए अर्धायु (t1/2) का व्यंजक:
👉 t1/2 = 0.693 / k
(स) 75% अभिक्रिया पूर्ण होने का समय
✅ सिद्ध होता है कि:
👉 t75% = 2t1/2
व्याख्या (Step by Step) 👉
(अ) संघट्ट आवृत्ति की सरल व्याख्या
• अभिक्रिया होने के लिए कणों का टकराना जरूरी है।
• एक निश्चित समय में जितने अधिक संघट्ट होंगे, अभिक्रिया की संभावना उतनी अधिक होगी।
✅ लेकिन हर संघट्ट प्रभावी (effective) नहीं होता।
(ब) प्रथम कोटि अभिक्रिया के अर्धायु का व्युत्पन्न
प्रथम कोटि अभिक्रिया का समाकलित वेग समीकरण:
👉 k = (2.303/t) log ([A]0 / [A]t)
अर्धायु पर,
👉 t = t1/2 तथा [A]t = [A]0/2
अब समीकरण में रखें:
👉 k = (2.303/t1/2) log ([A]0 / ([A]0/2))
👉 k = (2.303/t1/2) log 2
दिया है: log 2 = 0.3010
👉 k = (2.303 × 0.3010) / t1/2
👉 k = 0.693 / t1/2
अतः,
👉 t1/2 = 0.693 / k
✅ यही प्रथम कोटि अभिक्रिया का अर्धायु व्यंजक है।
(स) सिद्ध कीजिए: 75% अभिक्रिया पूर्ण होने का समय = 2 × अर्धायु
Step 1: 75% completion का मतलब
यदि 75% अभिक्रिया पूर्ण हो गई, तो 25% अभिकारक शेष है।
👉 [A]t = 25% of [A]0 = [A]0/4
Step 2: First-order equation में मान रखें
👉 t = (2.303/k) log ([A]0 / [A]t)
👉 t75% = (2.303/k) log ([A]0 / ([A]0/4))
👉 t75% = (2.303/k) log 4
अब,
👉 log 4 = log(2 × 2) = 2 log 2 = 2 × 0.3010 = 0.6020
तो,
👉 t75% = (2.303/k) × 0.6020
👉 t75% ≈ 1.386 / k
Step 3: अर्धायु से तुलना
प्रथम कोटि अभिक्रिया के लिए:
👉 t1/2 = 0.693/k
इसका दुगुना:
👉 2t1/2 = 2 × (0.693/k) = 1.386/k
जो कि t75% के बराबर है।
✅ अतः सिद्ध हुआ:
👉 t75% = 2t1/2
क्या आप जानते हैं? 🤔📌
✅
प्रथम कोटि अभिक्रिया
में हर अर्धायु के बाद अभिकारक की मात्रा आधी रह जाती है।
• 1 अर्धायु बाद → 50% शेष
• 2 अर्धायु बाद → 25% शेष (यानी 75% अभिक्रिया पूर्ण)
✅ इसी कारण 75% completion का समय अर्धायु का दुगुना आता है।
(18)
(अ)
बेकलाइट के निर्माण में प्रयुक्त एल्डिहाइड का नाम लिखिए।
(ब) ग्लूटेरिक अम्ल का IUPAC नाम लिखिए।
(स) रोजनमुंड अपचयन अभिक्रिया को उदाहरण की सहायता से समझाइए।
(ब) ग्लूटेरिक अम्ल का IUPAC नाम लिखिए।
(स) रोजनमुंड अपचयन अभिक्रिया को उदाहरण की सहायता से समझाइए।
Answer ✅
(अ) बेकलाइट के निर्माण में प्रयुक्त एल्डिहाइड
👉 फॉर्मैल्डिहाइड (Formaldehyde / मेथेनल)
(ब) ग्लूटेरिक अम्ल का IUPAC नाम
👉 पेंटेन-1,5-डायोइक अम्ल (Pentanedioic acid)
(स) रोजनमुंड अपचयन अभिक्रिया (Rosenmund Reduction)
✅ अम्ल क्लोराइड (acid chloride) का हाइड्रोजन की उपस्थिति में Pd/BaSO4 (poisoned catalyst) द्वारा अपचयन करके एल्डिहाइड प्राप्त किया जाता है, इसे रोजनमुंड अपचयन कहते हैं।
👉 सामान्य समीकरण:
R–COCl + H2 → R–CHO + HCl
Pd/BaSO4 की उपस्थिति में।
👉 उदाहरण:
C6H5COCl + H2 → C6H5CHO + HCl
(बेंजोयल क्लोराइड → बेंज़ैल्डिहाइड)
व्याख्या (Step by Step) 👉
(अ) बेकलाइट
• बेकलाइट एक
फिनॉल-फॉर्मैल्डिहाइड रेजिन
है।
✅ इसलिए इसमें प्रयुक्त aldehyde = formaldehyde (methanal)
(ब) ग्लूटेरिक अम्ल
• संरचना:
HOOC–(CH2)3–COOH
• कुल 5 carbon chain + दोनों सिरों पर –COOH
✅ इसलिए IUPAC नाम = pentanedioic acid
(स) रोजनमुंड अपचयन
• Acid chloride को सीधे alcohol तक reduce होने से रोकने के लिए
poisoned catalyst (Pd/BaSO4)
उपयोग करते हैं।
✅ इससे reduction aldehyde पर रुक जाती है।
क्या आप जानते हैं? 🤔📌
✅ Rosenmund reduction में catalyst को अक्सर
sulfur/quinoline
से और कम सक्रिय किया जाता है ताकि
over-reduction
न हो।
✅ यह विधि acid chloride → aldehyde conversion के लिए बहुत महत्वपूर्ण है।
अथवा
(अ)
खाद्य उद्योगों में सिरके के रूप में प्रयुक्त कार्बोक्सिलिक अम्ल का नाम लिखिए।
(ब) एडीपिक अम्ल का IUPAC नाम लिखिए।
(स) हेल-वोल्हार्ड-ज़ेलिन्स्की अभिक्रिया को उदाहरण की सहायता से समझाइए।
(ब) एडीपिक अम्ल का IUPAC नाम लिखिए।
(स) हेल-वोल्हार्ड-ज़ेलिन्स्की अभिक्रिया को उदाहरण की सहायता से समझाइए।
Answer ✅
(अ) सिरके में प्रयुक्त कार्बोक्सिलिक अम्ल
👉 एसीटिक अम्ल (Acetic acid / एथेनोइक अम्ल)
(ब) एडीपिक अम्ल का IUPAC नाम
👉 हेक्सेन-1,6-डायोइक अम्ल (Hexanedioic acid)
(स) हेल-वोल्हार्ड-ज़ेलिन्स्की (HVZ) अभिक्रिया
✅ जिन कार्बोक्सिलिक अम्लों में α-H (अल्फा हाइड्रोजन) उपस्थित होता है, वे Cl2/Br2 तथा लाल फॉस्फोरस (red P) / PBr3 की उपस्थिति में α-हैलोजन प्रतिस्थापन करते हैं। इस अभिक्रिया को हेल-वोल्हार्ड-ज़ेलिन्स्की अभिक्रिया कहते हैं।
👉 सामान्य रूप:
R–CH2–COOH → R–CHBr–COOH
👉 उदाहरण (एसीटिक अम्ल):
CH3COOH → CH2BrCOOH
Br2/Red,P की उपस्थिति में।
(ब्रोमोएसीटिक अम्ल)
व्याख्या (Step by Step) 👉
(अ) सिरका (Vinegar)
✅ सिरका मुख्यतः
एसीटिक अम्ल (CH3COOH)
का जलीय विलयन होता है।
इसलिए खाद्य उद्योग में उपयोग होने वाला acid = एसीटिक अम्ल।
(ब) एडीपिक अम्ल
एडीपिक अम्ल की संरचना:
👉 HOOC–(CH2)4–COOH
कुल कार्बन = 6
दो –COOH समूह = dioic acid
✅ इसलिए IUPAC नाम = Hexanedioic acid (हेक्सेन-1,6-डायोइक अम्ल)
(स) HVZ अभिक्रिया कैसे होती है?
• पहले acid का
acyl halide
बनता है
(PBr3 की मदद से)
• फिर α-carbon पर halogen जुड़ता है
• अंत में hydrolysis से α-halo carboxylic acid प्राप्त होता है
✅ शर्त: कार्बोक्सिलिक अम्ल में α-hydrogen होना चाहिए।
क्या आप जानते हैं? 🤔📌
✅
HVZ reaction
कार्बोक्सिलिक अम्लों के
α-carbon functionalisation
की महत्वपूर्ण विधि है।
✅ α-halo acids आगे amino acids बनाने में भी उपयोगी intermediates हो सकते हैं।
