उच्च माध्यमिक परीक्षा, 2026
SENIOR SECONDARY EXAMINATION, 2026
रसायन विज्ञान
CHEMISTRY
समय : 3 घंटे 15 मिनट
|
पूर्णांक : 56
Showing all questions
बहुविकल्पीय प्रश्न (i से xviii)
(1) निम्नलिखित प्रश्नों के सही विकल्प का चयन कीजिए और उनके उत्तर दीजिए।
(i)
आदर्श विलयन (Ideal Solution)
का उदाहरण है —
(अ) n-हेक्सेन व n-हेप्टेन का मिश्रण
(ब) एसीटोन व क्लोरोफॉर्म का मिश्रण
(स) एसीटोन व एथेनॉल का मिश्रण
(द) फिनॉल व एनिलीन का मिश्रण
(अ) n-हेक्सेन व n-हेप्टेन का मिश्रण
(ब) एसीटोन व क्लोरोफॉर्म का मिश्रण
(स) एसीटोन व एथेनॉल का मिश्रण
(द) फिनॉल व एनिलीन का मिश्रण
उत्तर ✅
सही विकल्प है —👉
(अ) n-हेक्सेन व n-हेप्टेन का मिश्रण ✅
व्याख्या (Step by Step) 👉
आदर्श विलयन
वह होता है जो
रॉल्ट के नियम (Raoult’s law)
का पूरी तरह पालन करे।
ऐसे विलयन में:
A–A, B–B और A–B के बीच आकर्षण बल लगभग एक जैसे होते हैं।
इसलिए:
ΔHmix ≈ 0 और ΔVmix ≈ 0 होता है।
n-हेक्सेन और n-हेप्टेन दोनों समान प्रकृति के अपध्रुवीय (non-polar) हाइड्रोकार्बन हैं, इनके बीच आकर्षण लगभग समान रहता है।
इसलिए इनका मिश्रण आदर्श विलयन का अच्छा उदाहरण माना जाता है।
बाकी विकल्प क्यों नहीं?
✅ एसीटोन + क्लोरोफॉर्म: इनके बीच हाइड्रोजन बॉन्डिंग बनती है → ऋणात्मक विचलन (negative deviation)
✅ एसीटोन + एथेनॉल: इंटरैक्शन बदल जाता है → आदर्श नहीं
✅ फिनॉल + एनिलीन: मजबूत H-बॉन्डिंग → आदर्श नहीं
क्या आप जानते हैं? 🤔📌
✅ आदर्श विलयन में
वाष्प दाब
का व्यवहार
“सीधा”
होता है, यानी
रॉल्ट के नियम
के अनुसार चलता है।
✅ परीक्षा में अक्सर बेंज़ीन + टोल्यून और n-हेक्सेन + n-हेप्टेन जैसे मिश्रण आदर्श विलयन के उदाहरण के रूप में पूछे जाते हैं।
(ii)
अधोलिखित में से
अधिकतम वान्ट हॉफ कारक (i)
मान वाला
प्रबल विद्युत अपघट्य
कौन-सा है? [½]
(अ) NaCl
(ब) KCl
(स) MgSO4
(द) K2SO4
(अ) NaCl
(ब) KCl
(स) MgSO4
(द) K2SO4
उत्तर ✅
सही विकल्प है —👉
(द) K2SO4 ✅
व्याख्या (Step by Step) 👉
वान्ट हॉफ कारक (i)
= घोल में 1 सूत्र इकाई टूटकर कुल कितने
आयन (कण)
बनाती है।
(प्रबल विद्युत अपघट्य में वियोजन लगभग पूरा मानते हैं।)
अब हर विकल्प का वियोजन देखें:
NaCl → Na+ + Cl−
➡️ कुल आयन = 2 ⇒ i = 2
KCl → K+ + Cl−
➡️ कुल आयन = 2 ⇒ i = 2
MgSO4 → Mg2+ + SO42−
➡️ कुल आयन = 2 ⇒ i = 2
K2SO4 → 2K+ + SO42−
➡️ कुल आयन = 3 ⇒ i = 3 (सबसे बड़ा)
इसलिए अधिकतम i वाला प्रबल विद्युत अपघट्य K2SO4 है।
क्या आप जानते हैं? 🤔📌
✅ सामान्य नियम:
जिस salt से जितने ज्यादा
आयन
बनेंगे, उसका
i
उतना ज्यादा होगा।
✅ जैसे AlCl3 → Al3+ + 3Cl−, इसलिए i = 4 (पूर्ण वियोजन मानें तो)।
(iii)
अधोलिखित में से
वैद्युतरोधी पदार्थ (Insulator)
कौन-सा है?
(अ) ग्रेफाइट
(ब) टेफलॉन
(स) सोडियम
(द) सिल्वर
(अ) ग्रेफाइट
(ब) टेफलॉन
(स) सोडियम
(द) सिल्वर
उत्तर ✅
सही विकल्प है —👉
(ब) टेफलॉन ✅
व्याख्या (Step by Step) 👉
वैद्युतरोधी पदार्थ
वे होते हैं जो
बिजली का प्रवाह
नहीं होने देते, क्योंकि इनमें
मुक्त इलेक्ट्रॉन (free electrons)
नहीं होते।
टेफलॉन (Teflon) एक प्लास्टिक/पॉलिमर है, इसमें मुक्त इलेक्ट्रॉन नहीं होते, इसलिए यह इन्सुलेटर है।
बाकी विकल्प क्यों नहीं?
✅ ग्रेफाइट में परतों के बीच मुक्त इलेक्ट्रॉन होते हैं, इसलिए यह चालक है।
✅ सोडियम धातु है, धातुएँ सामान्यतः अच्छी चालक होती हैं।
✅ सिल्वर (चाँदी) बहुत अच्छी विद्युत चालक धातु है।
क्या आप जानते हैं? 🤔📌
✅
टेफलॉन
का उपयोग
इलेक्ट्रिकल वायर की कोटिंग,
इन्सुलेशन
और
नॉन-स्टिक कुकवेयर
में भी किया जाता है।
(iv)
स्वर्ण (Gold)
सतह पर
HI
के
उत्प्रेरित वियोजन (catalysed decomposition)
हेतु अभिक्रिया की
कोटि
क्या है?
(अ) 0
(ब) 1
(स) 2
(द) 3
(अ) 0
(ब) 1
(स) 2
(द) 3
उत्तर ✅
सही विकल्प है —👉
(अ) 0 ✅ (शून्य कोटि)
व्याख्या (Step by Step) 👉
स्वर्ण सतह
पर
HI
का उत्प्रेरित वियोजन एक
सतही (surface)
अभिक्रिया है।
सतही अभिक्रियाओं में अक्सर ऐसा होता है कि सतह के सक्रिय स्थान (active sites) जल्दी भर जाते हैं।
जब सतह पूरी तरह भर जाती है, तब अभिक्रिया की गति HI की सांद्रता बढ़ाने से भी नहीं बढ़ती। यानी गति स्थिर (constant) हो जाती है।
इसलिए यह शून्य कोटि (Zero order) की अभिक्रिया मानी जाती है।
क्या आप जानते हैं? 🤔📌
✅ शून्य कोटि अभिक्रिया में:
दर = k
यानी गति केवल k पर निर्भर करती है, सांद्रता पर नहीं।
✅ इसी तरह की शून्य कोटि अभिक्रियाएँ अक्सर उत्प्रेरक सतह या फोटोकेमिकल परिस्थितियों में देखी जाती हैं।
(v)
वेग
=
K
[X]3/2
[Y]−1
उपयुक्त वेग व्यंजक के लिए अभिक्रिया की कुल कोटि क्या है?
(अ) 1/2
(ब) 1
(स) 3/2
(द) 5/2
उपयुक्त वेग व्यंजक के लिए अभिक्रिया की कुल कोटि क्या है?
(अ) 1/2
(ब) 1
(स) 3/2
(द) 5/2
उत्तर ✅
सही विकल्प है —👉
(अ) 1/2 ✅
व्याख्या (Step by Step) 👉
कुल कोटि (Overall order)
निकालने के लिए वेग व्यंजक में सभी
घातांकों (powers)
को जोड़ते हैं:
वेग = K [X]3/2 [Y]−1
कुल कोटि = (X का घातांक) + (Y का घातांक)
कुल कोटि = 3/2 + (−1)
कुल कोटि = 3/2 − 1 = 1/2
इसलिए सही विकल्प 1/2 है।
क्या आप जानते हैं? 🤔📌
✅
ऋणात्मक घातांक (negative power)
का मतलब होता है कि उस पदार्थ की
सांद्रता
बढ़ाने पर वेग
घट
सकता है।
✅ भिन्नात्मक कोटि (fractional order) भी हो सकती है, यह अक्सर जटिल अभिक्रियाओं (complex reactions) में दिखती है।
(vi)
अधोलिखित में से
संक्रमण तत्व (Transition Element)
कौन-सा है?
(अ) जिंक
(ब) कैडमियम
(स) सीरियम
(द) रदरफोर्डियम
(अ) जिंक
(ब) कैडमियम
(स) सीरियम
(द) रदरफोर्डियम
उत्तर ✅
सही विकल्प है —👉
(द) रदरफोर्डियम ✅
व्याख्या (Step by Step) 👉
संक्रमण तत्व
वे होते हैं जिनके परमाणु या उनके आयन में
d-ऑर्बिटल
आंशिक (partially) भरा
हुआ होता है।
अब विकल्पों को समझें:
✅ जिंक (Zn): इसका d-ऑर्बिटल पूरी तरह भरा d10 होता है, इसलिए इसे सामान्यतः संक्रमण तत्व नहीं माना जाता।
✅ कैडमियम (Cd): इसमें भी d-ऑर्बिटल d10 होता है, इसलिए यह भी संक्रमण तत्व नहीं है।
✅ सीरियम (Ce): यह लैंथेनाइड (f-ब्लॉक) का तत्व है, इसे मुख्य संक्रमण तत्व (d-ब्लॉक transition) नहीं माना जाता।
✅ रदरफोर्डियम (Rf): यह d-ब्लॉक (समूह 4) का तत्व है, इसलिए संक्रमण तत्व माना जाता है। ✅
क्या आप जानते हैं? 🤔📌
✅
Zn, Cd, Hg
d-ब्लॉक में होते हुए भी अक्सर
संक्रमण तत्व नहीं
माने जाते, क्योंकि इनके आयनों में d-ऑर्बिटल आमतौर पर
d10
(पूरी तरह भरा) रहता है।
✅ सीरियम जैसे तत्वों को कभी-कभी आंतरिक संक्रमण तत्व (Inner Transition Elements) भी कहा जाता है (क्योंकि ये f-ब्लॉक में आते हैं)।
(vii)
अधिकतम
अयुग्मित (unpaired) इलेक्ट्रॉन
वाला आयन कौन-सा है?
(अ) Ti2+
(ब) V2+
(स) Fe2+
(द) Ni2+
(अ) Ti2+
(ब) V2+
(स) Fe2+
(द) Ni2+
उत्तर ✅
सही विकल्प है —👉
(स) Fe2+ ✅
व्याख्या (Step by Step) 👉
अयुग्मित इलेक्ट्रॉन
निकालने के लिए पहले हर आयन का
d-इलेक्ट्रॉन कॉन्फ़िगरेशन
देखते हैं।
(धातु आयन बनाते समय पहले 4s के इलेक्ट्रॉन निकलते हैं, फिर 3d के।)
1) Ti (22): [Ar] 3d2 4s2
Ti2+:
4s के 2 निकलेंगे → [Ar] 3d2
➡️ d2 में 2 अयुग्मित इलेक्ट्रॉन
2) V (23): [Ar] 3d3 4s2
V2+:
4s के 2 निकलेंगे → [Ar] 3d3
➡️ d3 में 3 अयुग्मित इलेक्ट्रॉन
3) Fe (26): [Ar] 3d6 4s2
Fe2+:
4s के 2 निकलेंगे → [Ar] 3d6
➡️ d6 में (हंड के नियम से) 4 अयुग्मित इलेक्ट्रॉन ✅
4) Ni (28): [Ar] 3d8 4s2
Ni2+:
4s के 2 निकलेंगे → [Ar] 3d8
➡️ d8 में 2 अयुग्मित इलेक्ट्रॉन
✅ सबसे ज्यादा अयुग्मित इलेक्ट्रॉन Fe2+ (4 unpaired) में हैं।
क्या आप जानते हैं? 🤔📌
✅
d5
कॉन्फ़िगरेशन (जैसे
Mn2+)
में सबसे ज्यादा
5 अयुग्मित इलेक्ट्रॉन
होते हैं।
✅ अयुग्मित इलेक्ट्रॉन जितने ज्यादा, पदार्थ का चुंबकीय गुण (paramagnetism) उतना ज्यादा होता है।
(viii)
अभदन्ती (Ambidentate)
लिगाण्ड कौन-सा है?
(अ) H2O
(ब) NH3
(स) NO2−
(द) Cl−
(अ) H2O
(ब) NH3
(स) NO2−
(द) Cl−
उत्तर ✅
सही विकल्प है —👉
(स) NO2− ✅
व्याख्या (Step by Step) 👉
अभदन्ती (Ambidentate) लिगाण्ड
वह होता है जो
दो अलग-अलग परमाणुओं (donor atoms)
में से किसी एक के द्वारा धातु से जुड़ सकता है
(एक समय में एक ही जगह से जुड़ता है)।
NO2− (नाइट्राइट आयन) दो तरीकों से जुड़ सकता है:
✅ N (नाइट्रोजन) से जुड़कर → nitro
M–NO2
✅ O (ऑक्सीजन) से जुड़कर → nitrito
M–ONO
इसलिए NO2− अभदन्ती लिगाण्ड है। ✅
बाकी विकल्प क्यों नहीं?
✅ H2O: केवल O से जुड़ता है (एक ही donor atom)
✅ NH3: केवल N से जुड़ता है
✅ Cl−: केवल Cl से जुड़ता है
क्या आप जानते हैं? 🤔📌
✅ एक और बहुत प्रसिद्ध अभदन्ती लिगाण्ड है:
SCN−
✅ S से जुड़े तो → thiocyanato
M–SCN
✅ N से जुड़े तो → isothiocyanato
M–NCS
(ix)
[Pt(NH3)2Cl(NO2)]
संकुल में
Pt की समन्वय संख्या (Coordination Number)
क्या है?
(अ) 3
(ब) 4
(स) 5
(द) 6
(अ) 3
(ब) 4
(स) 5
(द) 6
उत्तर ✅
सही विकल्प है —👉
(ब) 4 ✅
व्याख्या (Step by Step) 👉
समन्वय संख्या
का मतलब होता है:
केंद्रीय धातु (यहाँ
Pt)
से कुल कितने
दाता परमाणु (donor atoms)
सीधे जुड़े हैं।
अब संकुल में जुड़े लिगाण्ड गिनते हैं:
✅ NH3 = 2 (दो अमोनिया, हर एक 1-1 दाता परमाणु से जुड़ता है) → 2 donor
✅ Cl− = 1 (एक दाता परमाणु) → 1 donor
✅ NO2− = 1 (अभदन्ती है, लेकिन एक समय में एक ही परमाणु से जुड़ता है) → 1 donor
कुल donor atoms = 2 + 1 + 1 = 4
इसलिए Pt की समन्वय संख्या = 4 ✅
क्या आप जानते हैं? 🤔📌
✅
Pt(II)
के बहुत से संकुलों की
समन्वय संख्या
4
होती है और उनका
ज्यामिति (geometry)
अक्सर
वर्ग-समतलीय (Square planar)
होती है।
(x)
अधोलिखित में से
सर्वाधिक कार्बन–हैलोजन (C–X) आबंध लंबाई
वाला यौगिक कौन-सा है?
(अ) CH3F
(ब) CH3Cl
(स) CH3Br
(द) CH3I
(अ) CH3F
(ब) CH3Cl
(स) CH3Br
(द) CH3I
उत्तर ✅
सही विकल्प है —👉
(द) CH3I ✅
व्याख्या (Step by Step) 👉
C–X आबंध लंबाई
मुख्यतः हैलोजन के
परमाणु आकार (atomic size)
पर निर्भर करती है।
हैलोजन समूह में नीचे जाते हुए आकार बढ़ता है:
F < Cl < Br < I
जब हैलोजन का आकार बड़ा होता है, तो कार्बन से दूरी ज्यादा हो जाती है, इसलिए आबंध लंबाई बढ़ती है।
इसलिए आबंध लंबाई का क्रम होगा:
C–F < C–Cl < C–Br < C–I
✅ सबसे लंबी आबंध लंबाई CH3I में होगी।
क्या आप जानते हैं? 🤔📌
✅ आबंध लंबाई जितनी ज्यादा, आबंध आमतौर पर उतना
कमज़ोर
होता है।
✅ इसलिए सामान्यतः C–I सबसे कमजोर और C–F सबसे मजबूत माना जाता है।
(xi)
2CHCl3 + O2 —(प्रकाश)→ [A] + 2HCl
उपर्युक्त अभिक्रिया में उत्पाद [A] क्या है?
(अ) फॉस्फीन
(ब) फॉस्जीन
(स) मेथिलीन क्लोराइड
(द) कार्बन टेट्राक्लोराइड
उपर्युक्त अभिक्रिया में उत्पाद [A] क्या है?
(अ) फॉस्फीन
(ब) फॉस्जीन
(स) मेथिलीन क्लोराइड
(द) कार्बन टेट्राक्लोराइड
उत्तर ✅
सही विकल्प है —👉
(ब) फॉस्जीन (COCl2) ✅
व्याख्या (Step by Step) 👉
क्लोरोफॉर्म (CHCl3)
जब
प्रकाश
की उपस्थिति में
ऑक्सीजन
के साथ अभिक्रिया करता है, तो उसका ऑक्सीकरण होकर
फॉस्जीन (COCl2)
बनता है और साथ में
HCl
निकलता है।
सरल रूप में अभिक्रिया:
2CHCl3 + O2 → 2COCl2 + 2HCl
इसलिए [A] = COCl2 (फॉस्जीन)
क्या आप जानते हैं? 🤔📌
✅
फॉस्जीन (COCl2)
बहुत
विषैला (toxic)
गैस है।
✅ इसी कारण क्लोरोफॉर्म को हमेशा अँधेरी बोतल में और अक्सर थोड़ी मात्रा में अल्कोहल (ethanol) मिलाकर रखा जाता है, ताकि फॉस्जीन बनने का खतरा कम हो जाए।
(xii)
काठ स्पिरिट (Wood Spirit)
कौन-सा है?
(अ) मेथेनॉल
(ब) एथेनॉल
(स) प्रोपेनॉल
(द) एसीटोन
(अ) मेथेनॉल
(ब) एथेनॉल
(स) प्रोपेनॉल
(द) एसीटोन
उत्तर ✅
सही विकल्प है —👉
(अ) मेथेनॉल ✅
व्याख्या (Step by Step) 👉
काठ स्पिरिट
का मतलब है
मेथेनॉल
(CH3OH)।
पहले समय में मेथेनॉल को लकड़ी के शुष्क आसवन (dry distillation of wood) से बनाया जाता था, इसलिए इसे काठ स्पिरिट कहा गया।
बाकी विकल्प
✅ एथेनॉल को सामान्यतः अल्कोहल/स्पिरिट (पीने वाला अल्कोहल) कहा जाता है (शुद्ध रूप में)।
✅ प्रोपेनॉल एक अन्य अल्कोहल है, लेकिन “काठ स्पिरिट” नहीं।
✅ एसीटोन अल्कोहल नहीं, यह कीटोन है।
क्या आप जानते हैं? 🤔📌
✅
मेथेनॉल
बहुत
विषैला
होता है। थोड़ी मात्रा भी शरीर में जाकर
आँखों की रोशनी
को नुकसान पहुँचा सकती है।
✅ परीक्षा में “काठ स्पिरिट = मेथेनॉल” अक्सर सीधा पूछा जाता है।
(xiii)
द्वितीयक (Secondary) ऐल्कोहॉल
कौन-सा है?
(अ) एथिल ऐल्कोहॉल
(ब) एथिलीन ग्लाइकोल
(स) आइसोप्रोपिल ऐल्कोहॉल
(द) आइसोब्यूटिल ऐल्कोहॉल
(अ) एथिल ऐल्कोहॉल
(ब) एथिलीन ग्लाइकोल
(स) आइसोप्रोपिल ऐल्कोहॉल
(द) आइसोब्यूटिल ऐल्कोहॉल
उत्तर ✅
सही विकल्प है —👉
(स) आइसोप्रोपिल ऐल्कोहॉल ✅
व्याख्या (Step by Step) 👉
द्वितीयक ऐल्कोहॉल
वह होता है जिसमें
–OH
समूह जिस कार्बन पर लगा हो, वह कार्बन
दो अन्य कार्बन
परमाणुओं से जुड़ा हो।
अब विकल्प देखें:
✅ एथिल ऐल्कोहॉल (C2H5OH): –OH वाला कार्बन सिर्फ एक कार्बन से जुड़ा होता है → प्राथमिक (Primary)
✅ एथिलीन ग्लाइकोल (HO–CH2–CH2–OH): दोनों –OH CH2 पर हैं → दोनों प्राथमिक
✅ आइसोप्रोपिल ऐल्कोहॉल (CH3–CHOH–CH3): –OH वाला कार्बन दो कार्बन (दो CH3) से जुड़ा है → द्वितीयक (Secondary) ✅
✅ आइसोब्यूटिल ऐल्कोहॉल ((CH3)2CH–CH2OH): –OH CH2 पर है → प्राथमिक (Primary)
इसलिए सही विकल्प आइसोप्रोपिल ऐल्कोहॉल है।
क्या आप जानते हैं? 🤔📌
✅
द्वितीयक ऐल्कोहॉल
का ऑक्सीकरण करने पर सामान्यतः
कीटोन (Ketone)
बनता है।
उदाहरण: आइसोप्रोपिल ऐल्कोहॉल → एसीटोन (Ketone)
(xiv)
अधोलिखित में से
दुर्बलतम अम्ल (सबसे कमजोर acid)
कौन-सा है?
(अ) HCOOH
(ब) CH3COOH
(स) FCH2COOH
(द) ClCH2COOH
(अ) HCOOH
(ब) CH3COOH
(स) FCH2COOH
(द) ClCH2COOH
उत्तर ✅
सही विकल्प है —👉
(ब) CH3COOH (एसीटिक अम्ल) ✅
व्याख्या (Step by Step) 👉
कार्बोक्सिलिक अम्ल (R–COOH)
की अम्लीय शक्ति
R समूह के इंडक्टिव प्रभाव (+I / −I)
पर निर्भर करती है।
−I (इलेक्ट्रॉन खींचने वाले) समूह अम्ल को ज्यादा प्रबल बनाते हैं, क्योंकि वे कार्बोक्सिलेट आयन (RCOO−) को स्थिर करते हैं।
+I (इलेक्ट्रॉन देने वाले) समूह अम्ल को कमजोर बनाते हैं, क्योंकि वे कार्बोक्सिलेट आयन को कम स्थिर करते हैं।
अब विकल्प देखें:
✅ FCH2COOH और ClCH2COOH में F और Cl −I प्रभाव दिखाते हैं → ये अधिक प्रबल अम्ल होंगे।
✅ HCOOH (फॉर्मिक अम्ल) में कोई अल्किल समूह नहीं है, यह एसीटिक अम्ल से प्रबल होता है।
✅ CH3COOH (एसीटिक अम्ल) में CH3 समूह +I प्रभाव देता है → अम्लीयता कम हो जाती है।
इसलिए सबसे दुर्बल (weakest) अम्ल = CH3COOH ✅
क्या आप जानते हैं? 🤔📌
✅ हैलोजन वाले अम्लों में सामान्यतः अम्लीयता का क्रम:
FCH2COOH > ClCH2COOH > CH3COOH
क्योंकि F का −I प्रभाव सबसे ज्यादा होता है।
(xv)
तृतीयक (Tertiary) एमीन
कौन-सा है?
(अ) n-प्रोपाइलएमीन
(ब) आइसोप्रोपाइलएमीन
(स) एथिलमिथाइलएमीन
(द) ट्राइमेथिलएमीन
(अ) n-प्रोपाइलएमीन
(ब) आइसोप्रोपाइलएमीन
(स) एथिलमिथाइलएमीन
(द) ट्राइमेथिलएमीन
उत्तर ✅
सही विकल्प है —👉
(द) ट्राइमेथिलएमीन ✅
व्याख्या (Step by Step) 👉
एमीन का प्रकार इस बात पर निर्भर करता है कि
नाइट्रोजन (N)
से कितने
अल्किल/एरिल समूह
जुड़े हैं:
प्राथमिक (1°) एमीन: R–NH2 (N से 1 कार्बन समूह)
द्वितीयक (2°) एमीन: R2NH (N से 2 कार्बन समूह)
तृतीयक (3°) एमीन: R3N ✅ (N से 3 कार्बन समूह)
अब विकल्प देखें:
✅ n-प्रोपाइलएमीन (C3H7NH2) → 1°
✅ आइसोप्रोपाइलएमीन (C3H7NH2) → 1°
✅ एथिलमिथाइलएमीन (C2H5NHCH3) → 2°
✅ ट्राइमेथिलएमीन ((CH3)3N) → 3° ✅
इसलिए सही विकल्प ट्राइमेथिलएमीन है।
क्या आप जानते हैं? 🤔📌
✅ तृतीयक एमीन में
N–H बंध नहीं
होता, इसलिए ये
आंतरिक (self) हाइड्रोजन बॉन्डिंग
नहीं कर पाते।
✅ ट्राइमेथिलएमीन की गंध अक्सर मछली जैसी (fishy smell) होती है।
(xvi)
एमीन में
नाइट्रोजन (N)
परमाणु की
संकरित अवस्था (Hybridisation)
क्या होती है?
(अ) sp
(ब) sp2
(स) sp3
(द) sp3d2
(अ) sp
(ब) sp2
(स) sp3
(द) sp3d2
उत्तर ✅
सही विकल्प है —👉
(स) sp3 ✅
व्याख्या (Step by Step) 👉
एमीन
(R–NH2, R2NH, R3N)
में नाइट्रोजन के पास आमतौर पर:
✅ 3 σ (सिग्मा) बंध होते हैं
✅ और 1 अकेला इलेक्ट्रॉन युग्म (lone pair) होता है
यानी कुल 4 इलेक्ट्रॉन-युग्म क्षेत्र (3 बंध + 1 lone pair) होते हैं।
4 क्षेत्र ⇒ sp3 संकरण
इस कारण अमीन का आकार त्रिकोणीय पिरामिडीय (trigonal pyramidal) होता है।
क्या आप जानते हैं? 🤔📌
✅
अमोनिया (NH3)
में भी N की संकरित अवस्था
sp3
होती है।
✅ lone pair के कारण N–H (या N–C) बंध कोण 109.5° से थोड़ा कम (~107°) हो जाता है।
(xvii)
पोलिसैकेराइड (Polysaccharide)
कौन-सा है?
(अ) राइबोस
(ब) लैक्टोस
(स) सुक्रोस
(द) ग्लाइकोजन
(अ) राइबोस
(ब) लैक्टोस
(स) सुक्रोस
(द) ग्लाइकोजन
उत्तर ✅
सही विकल्प है —👉
(द) ग्लाइकोजन ✅
व्याख्या (Step by Step) 👉
पोलिसैकेराइड
वे कार्बोहाइड्रेट होते हैं जो बहुत सारे
मोनोसैकेराइड इकाइयों
से मिलकर बने होते हैं (लंबी श्रृंखला/पॉलिमर)।
अब विकल्प देखें:
✅ राइबोस → मोनोसैकेराइड (एक ही शर्करा इकाई)
✅ लैक्टोस → डाइसैकेराइड (ग्लूकोज़ + गैलेक्टोज़)
✅ सुक्रोस → डाइसैकेराइड (ग्लूकोज़ + फ्रक्टोज़)
✅ ग्लाइकोजन → पोलिसैकेराइड (बहुत सारी ग्लूकोज़ इकाइयाँ) ✅
इसलिए सही उत्तर ग्लाइकोजन है।
क्या आप जानते हैं? 🤔📌
✅
ग्लाइकोजन
को
“Animal starch”
भी कहा जाता है क्योंकि यह जानवरों में
ऊर्जा का भंडार
होता है।
✅ यह मुख्यतः यकृत (Liver) और मांसपेशियों (Muscles) में संग्रहित रहता है।
(2) रिक्त स्थान भरें : (i से x)
(i)
ताप बढ़ाने पर,
द्रवों में गैसों की विलेयता
________ है।
उत्तर ✅
घटती है ✅ (कम होती है)
व्याख्या (Step by Step) 👉
जब हम
ताप (Temperature)
बढ़ाते हैं, तो गैस के कणों की
गतिज ऊर्जा
बढ़ जाती है।
वे द्रव में टिकने की बजाय जल्दी बाहर निकलने लगते हैं, इसलिए द्रव में गैस की विलेयता कम हो जाती है।
उदाहरण: गर्म पानी में ठंडे पानी की तुलना में ऑक्सीजन/कार्बन डाइऑक्साइड कम घुलती है।
क्या आप जानते हैं? 🤔📌
✅ गर्मियों में तालाब/नदियों में पानी गर्म होने से
O2
की विलेयता
घटती
है, इसलिए मछलियों को कभी-कभी
ऑक्सीजन की कमी
महसूस हो सकती है।
(ii)
मोलल उन्नयन स्थिरांक
(Kb)
की इकाई ________ है।
उत्तर ✅
Kb की इकाई =
K kg mol−1 ✅
(या °C kg mol−1 भी लिख सकते हैं)
व्याख्या (Step by Step) 👉
उबलांक उन्नयन का सूत्र होता है:
ΔTb = Kb × m
जहाँ,
ΔTb = उबलांक में वृद्धि (इकाई: K या °C)
m = मोललता (इकाई: mol kg−1)
तो,
Kb = ΔTb / m
इकाई बनेगी:
(K) / (mol kg−1) = K kg mol−1
इसलिए Kb की इकाई K kg mol−1 होती है।
क्या आप जानते हैं? 🤔📌
✅
Kb
भी
विलायक (solvent)
पर निर्भर करता है,
विलेय (solute)
पर नहीं।
✅ पानी (H2O) के लिए Kb लगभग 0.512 K kg mol−1 होता है।
(iii)
वैद्युत अपघटनी (Electrolytic) विलयनों
की
चालकता
ताप बढ़ाने पर ________ है।
उत्तर ✅
बढ़ती है ✅ (वृद्धि होती है)
व्याख्या (Step by Step) 👉
वैद्युत अपघटनी विलयनों (जैसे
NaCl,
HCl,
आदि के घोल) में बिजली का प्रवाह
आयनों (ions)
की वजह से होता है।
जब ताप बढ़ाया जाता है, तो:
✅ आयनों की गतिशीलता (mobility) बढ़ जाती है
✅ द्रव की श्यानता (viscosity) घट जाती है
✅ आयन अधिक आसानी से चल पाते हैं
इसलिए चालकता बढ़ जाती है।
क्या आप जानते हैं? 🤔📌
✅
धातुओं
में ताप बढ़ाने पर चालकता अक्सर
घटती
है, लेकिन
इलेक्ट्रोलाइटिक विलयनों
में
बढ़ती
है।
✅ यही वजह है कि कई घोल गर्म करने पर बेहतर कंडक्ट करते हैं।
(iv)
यदि किसी अभिक्रिया के लिए
वेग स्थिरांक (k)
का मान
1.75 × 10−5
L mol−1 s−1
पाया गया, तो अभिक्रिया की कोटि ________ होगी।
उत्तर ✅
द्वितीय कोटि (Second order) ✅
व्याख्या (Step by Step) 👉
वेग स्थिरांक k
की इकाई से अभिक्रिया की
कोटि
पता चल जाती है।
प्रथम कोटि के लिए k की इकाई होती है: s−1
द्वितीय कोटि के लिए k की इकाई होती है: L mol−1 s−1 ✅
शून्य कोटि के लिए k की इकाई होती है: mol L−1 s−1
यहाँ दी गई इकाई L mol−1 s−1 है, इसलिए अभिक्रिया द्वितीय कोटि की होगी।
क्या आप जानते हैं? 🤔📌
✅
कोटि (Order)
हमेशा
प्रयोग
से तय होती है, यह रासायनिक समीकरण के
गुणांकों के बराबर जरूरी नहीं
होती।
(v)
प्रथम संक्रमण श्रेणी (First Transition Series)
में सबसे कम
कणनन एन्थैल्पी (Atomization Enthalpy)
मान वाला तत्व ________ है।
उत्तर ✅
जिंक (Zn) ✅
व्याख्या (Step by Step) 👉
कणनन एन्थैल्पी
का मतलब होता है:
किसी धातु को ठोस अवस्था से गैसीय परमाणुओं में बदलने के लिए जितनी ऊर्जा चाहिए।
प्रथम संक्रमण श्रेणी में Zn (जिंक) के इलेक्ट्रॉन विन्यास में 3d10 4s2 होता है।
यहाँ d-कक्ष पूरी तरह भरा (full-filled) होता है, इसलिए:
धात्विक बंधन (metallic bonding) तुलनात्मक रूप से कमजोर हो जाता है
और परमाणुओं को अलग करने में कम ऊर्जा लगती है
इसी कारण Zn की कणनन एन्थैल्पी सबसे कम मानी जाती है।
क्या आप जानते हैं? 🤔📌
इसी श्रेणी में
Mn (मैंगनीज़)
की
कणनन एन्थैल्पी
भी अपेक्षाकृत कम होती है, क्योंकि इसमें
3d5
(half-filled)
स्थिरता मिलती है।
सामान्य तौर पर धात्विक बंधन जितना मजबूत, कणनन एन्थैल्पी उतनी अधिक होती है।
(vi)
जिन
त्रिविम समावयवियों
का संबंध परस्पर
अध्यारोपित न हो सकने वाले
दर्पण प्रतिबिंबों
की तरह होता है, उन्हें ________ कहते हैं।
उत्तर ✅
एनेन्शियोमर (Enantiomers) ✅
(हिंदी में: दर्पण-प्रतिबिंब समावयवी)
व्याख्या (Step by Step) 👉
कुछ यौगिकों के दो
त्रिविम (3D)
रूप होते हैं जो एक-दूसरे के
दर्पण प्रतिबिंब
तो होते हैं, लेकिन एक-दूसरे पर पूरी तरह
चढ़ाए (superimpose)
नहीं जा सकते।
ठीक वैसे ही जैसे आपका बायाँ हाथ और दायाँ हाथ दिखने में समान होते हैं, पर एक-दूसरे पर पूरी तरह नहीं बैठते।
ऐसे समावयवियों को एनेन्शियोमर कहते हैं।
क्या आप जानते हैं? 🤔📌
एनेन्शियोमर
सामान्यतः
समतल ध्रुवीकृत प्रकाश (plane polarized light)
को घुमाते हैं।
एक दाईं ओर घुमाए तो दक्षिणावर्त (+)
दूसरा बाईं ओर घुमाए तो वामावर्त (−)
एनेन्शियोमर बनने का मुख्य कारण अक्सर काइरल कार्बन (चिरल/असममित कार्बन) होता है।
(vii)
ऐलिल ब्रोमाइड (Allyl bromide)
का
रासायनिक सूत्र
________ है।
उत्तर ✅
CH2=CH–CH2Br ✅
(अर्थात C3H5Br)
व्याख्या (Step by Step) 👉
ऐलिल (Allyl)
समूह का ढांचा होता है:
CH2=CH–CH2–
जब इसी ऐलिल समूह के साथ Br जुड़ जाता है, तो यौगिक बनता है:
CH2=CH–CH2Br
इसी को ऐलिल ब्रोमाइड कहते हैं।
क्या आप जानते हैं? 🤔📌
ऐलिल ब्रोमाइड
में
Br
जिस कार्बन पर होता है, वह
डबल बॉन्ड के पास वाला कार्बन
(allylic carbon)
होता है।
ऐलिल यौगिकों में बना allyl carbocation/allyl radical resonance से स्थिर होता है, इसलिए कई अभिक्रियाएँ तेजी से होती हैं।
(viii)
जैविक प्रतिरक्षों (biological specimens)
के
परिरक्षण
में प्रयुक्त
फॉर्मेल्डिहाइड
का
40% जलीय विलयन
________ कहलाता है।
उत्तर ✅
फॉर्मेलिन (Formalin) ✅
व्याख्या (Step by Step) 👉
फॉर्मेल्डिहाइड (HCHO)
का जब लगभग
40% जलीय विलयन
बनाया जाता है, तो उसे
फॉर्मेलिन
कहा जाता है।
इसे जैविक नमूनों/टिश्यू को खराब होने से बचाने (preserve) के लिए प्रयोग किया जाता है, क्योंकि यह सूक्ष्मजीवों की वृद्धि रोकता है और ऊतकों को संरक्षित करता है।
क्या आप जानते हैं? 🤔📌
फॉर्मेलिन
का प्रयोग
प्रयोगशालाओं,
अस्पतालों
और
म्यूज़ियम
में नमूनों को लंबे समय तक सुरक्षित रखने के लिए किया जाता है।
फॉर्मेल्डिहाइड की गंध तेज होती है और इसे सावधानी से संभालना चाहिए।
(ix)
ट्राइमिथाइलएमीन (Trimethylamine)
की
आकृति
________ होती है।
उत्तर ✅
त्रिकोणीय पिरामिडीय (Trigonal pyramidal) ✅
व्याख्या (Step by Step) 👉
ट्राइमिथाइलएमीन
का सूत्र
(CH3)3N
होता है।
नाइट्रोजन (N) के चारों ओर कुल 4 इलेक्ट्रॉन-युग्म क्षेत्र होते हैं:
3 σ बंध (तीन CH3 समूहों के साथ)
1 अकेला इलेक्ट्रॉन युग्म (lone pair)
4 क्षेत्र होने पर N की संकरित अवस्था sp3 होती है।
लेकिन lone pair होने की वजह से आकृति पूर्ण चतुष्फलकीय (tetrahedral) नहीं दिखती, बल्कि त्रिकोणीय पिरामिडीय बनती है।
क्या आप जानते हैं? 🤔📌
NH3
(अमोनिया)
की आकृति भी
त्रिकोणीय पिरामिडीय
होती है, कारण वही
lone pair
है।
अगर lone pair न हो (जैसे CH4 ), तो आकृति चतुष्फलकीय (tetrahedral) होती है।
(x)
विटामिन
________ की कमी से
स्कर्वी (Scurvy)
रोग होता है।
उत्तर ✅
विटामिन C ✅
(एस्कॉर्बिक अम्ल / Ascorbic acid)
व्याख्या (Step by Step) 👉
स्कर्वी (Scurvy)
रोग शरीर में
विटामिन C
की कमी से होता है।
विटामिन C शरीर में कोलेजन (Collagen) बनाने में जरूरी होता है। कोलेजन एक ऐसा प्रोटीन है जो:
मसूड़ों, त्वचा और रक्त वाहिकाओं को मजबूत रखता है
घाव भरने में मदद करता है
इसलिए विटामिन C की कमी होने पर अक्सर:
मसूड़ों से खून आना
घाव देर से भरना
कमजोरी/थकान जैसी समस्याएँ दिखती हैं।
क्या आप जानते हैं? 🤔📌
विटामिन C
के अच्छे स्रोत:
आँवला,
नींबू,
संतरा,
अमरूद,
टमाटर
आदि।
पुराने समय में समुद्री यात्राओं में ताजे फल-सब्जियाँ न मिलने से नाविकों में स्कर्वी ज्यादा होता था।
(3) अतिलघुत्तरात्मक प्रश्न: (i to x)
(निम्नलिखित प्रश्नों के उत्तर एक शब्द या एक पंक्ति में दीजिए)
(i)
नाइट्रोजन गैस
में
क्लोरोफॉर्म
के
गैसीय विलयन
में
विलेय
तथा
विलायक
लिखिए।
उत्तर ✅
विलेय (Solute):
क्लोरोफॉर्म (CHCl3)
विलायक (Solvent): नाइट्रोजन गैस (N2)
विलायक (Solvent): नाइट्रोजन गैस (N2)
व्याख्या (Step by Step) 👉
जिस पदार्थ की मात्रा अधिक होती है उसे
विलायक
कहते हैं, और जो कम मात्रा में घुलता/मिश्रित होता है उसे
विलेय
कहते हैं।
यहाँ “नाइट्रोजन गैस में क्लोरोफॉर्म का विलयन” लिखा है, मतलब नाइट्रोजन मुख्य माध्यम है, इसलिए वही विलायक होगा और क्लोरोफॉर्म विलेय ।
क्या आप जानते हैं? 🤔📌
गैसीय विलयनों
में भी वही नियम चलता है:
अधिक मात्रा वाला = विलायक,
कम मात्रा वाला = विलेय।
(ii)
मक्यूरी (Mercury) सेल
में प्रयुक्त
एनोड
का नाम लिखिए।
उत्तर ✅
जिंक–अमलगम (Zinc amalgam) ✅
(अर्थात Zn–Hg)
व्याख्या (Step by Step) 👉
मक्यूरी सेल
में
एनोड
पर
ऑक्सीकरण (oxidation)
होता है।
यहाँ जिंक को पारा (Hg) के साथ मिलाकर जिंक-अमलगम बनाया जाता है, ताकि जिंक की सतह स्थिर रहे और सेल अच्छी तरह काम करे।
इसलिए एनोड = जिंक–अमलगम (Zn–Hg) होता है।
क्या आप जानते हैं? 🤔📌
मक्यूरी सेल
का वोल्टेज लगभग
स्थिर
रहता है
(लगभग 1.35 V)
इसलिए इसे पहले
घड़ियों, कैमरों
आदि में इस्तेमाल किया जाता था।
(iii)
Ni(CO)4
में
निकेल (Ni)
की
ऑक्सीकरण अवस्था
लिखिए।
उत्तर ✅
0 (शून्य) ✅
व्याख्या (Step by Step) 👉
CO (कार्बोनाइल)
एक
उदासीन (neutral)
लिगैण्ड है, इसका आवेश
0
होता है।
Ni(CO)4 पूरा संकुल भी तटस्थ है, यानी कुल आवेश 0 है।
मान लें Ni की ऑक्सीकरण अवस्था = x
तो, x + 4(0) = 0
x = 0
इसलिए Ni की ऑक्सीकरण अवस्था 0 है।
क्या आप जानते हैं? 🤔📌
Ni(CO)4
एक
कार्बोनाइल संकुल
है और यह सामान्य ताप पर
उड़नशील (volatile)
भी होता है।
CO लिगाण्ड “π-बैक बॉन्डिंग” के कारण धातु से मजबूत बंध बनाता है, इसलिए ऐसे संकुल काफी स्थिर हो सकते हैं।
(iv)
‘प्रचक्रण मात्र’ (Spin-only)
से
चुम्बकीय आघूर्ण
ज्ञात करने का
सूत्र
लिखिए।
उत्तर ✅
μ = √(n(n+2)) BM ✅
व्याख्या (Step by Step) 👉
यहाँ,
μ = चुम्बकीय आघूर्ण (Magnetic Moment)
n = अयुग्मित (unpaired) इलेक्ट्रॉनों की संख्या
BM = बोहर मैग्नेटॉन (Bohr Magneton)
मतलब: जितने ज्यादा अयुग्मित इलेक्ट्रॉन, उतना ज्यादा चुम्बकीय आघूर्ण ।
क्या आप जानते हैं? 🤔📌
अगर
n = 0
हो, तो
μ = 0 BM
होता है और पदार्थ
अचुम्बकीय (diamagnetic)
कहलाता है।
अगर n > 0 हो, तो पदार्थ पराचुम्बकीय (paramagnetic) होता है।
(v)
निम्न प्रचक्रण संकुल (Low spin complex)
का कोई एक
उदाहरण
लिखिए।
उत्तर ✅
[Fe(CN)6]4− ✅
(फेरोसाइनाइड संकुल)
व्याख्या (Step by Step) 👉
Low spin complex
तब बनता है जब लिगैण्ड
प्रबल क्षेत्र (strong field)
वाला हो, जैसे
CN−,
CO
आदि।
मजबूत क्षेत्र लिगैण्ड इलेक्ट्रॉनों का युग्मीकरण (pairing) करवा देता है, इसलिए अयुग्मित इलेक्ट्रॉन कम हो जाते हैं और संकुल low spin कहलाता है।
क्या आप जानते हैं? 🤔📌
CN−
और
CO
को
strong field ligand
माना जाता है, इसलिए इनके संकुल अक्सर
low spin
होते हैं।
H2O, F−, Cl− जैसे लिगैण्ड कमजोर क्षेत्र वाले होते हैं, इनके संकुल अक्सर high spin होते हैं।
(vi)
निम्नलिखित यौगिकों को
SN2
अभिक्रिया के प्रति
अभिक्रियाशीलता के बढ़ते क्रम
में व्यवस्थित कीजिए:
CH3–CH2–CH(Br)–CH3
(CH3)3C–Br
CH3–CH2–CH2–CH2–Br
CH3–CH2–CH(Br)–CH3
(CH3)3C–Br
CH3–CH2–CH2–CH2–Br
उत्तर ✅
(CH3)3C–Br
<
CH3–CH2–CH(Br)–CH3
<
CH3–CH2–CH2–CH2–Br ✅
यानी: तृतीयक < द्वितीयक < प्राथमिक (SN2 के लिए)
व्याख्या (Step by Step) 👉
SN2
अभिक्रिया
एक ही चरण (one-step)
में होती है और इसमें न्यूक्लियोफाइल
पीछे की तरफ से (backside attack)
आता है।
इसलिए जहाँ भीड़ (steric hindrance) ज्यादा होती है, वहाँ SN2 धीमी हो जाती है।
(CH3)3C–Br = तृतीयक (सबसे ज्यादा भीड़) → सबसे कम SN2
CH3–CH2–CH(Br)–CH3 = द्वितीयक → बीच में
CH3–CH2–CH2–CH2–Br = प्राथमिक (कम भीड़) → सबसे ज्यादा SN2
क्या आप जानते हैं? 🤔📌
SN2
में
प्राथमिक
>
द्वितीयक
>>
तृतीयक
(लगभग नहीं होती)
तृतीयक हैलाइड अक्सर SN2 की जगह SN1 या elimination ज्यादा देते हैं।
(vii)
एथिल ऐल्कोहॉल (एथेनॉल)
की
वाष्प
को
573 K
पर
तप्त कॉपर
के ऊपर से प्रवाहित किया जाता है, तो प्राप्त
उत्पाद
का नाम लिखिए।
उत्तर ✅
एसीटैल्डिहाइड (एथेनल) ✅
व्याख्या (Step by Step) 👉
573 K
पर
तप्त कॉपर
एथेनॉल
का
डीहाइड्रोजनेशन (Dehydrogenation)
कर देता है, यानी हाइड्रोजन निकल जाता है:
CH3CH2OH —(Cu, 573 K)→ CH3CHO + H2
इसलिए उत्पाद बनता है: एथेनल (एसीटैल्डिहाइड)
क्या आप जानते हैं? 🤔📌
यही अभिक्रिया अगर
Cu
की जगह
Al2O3
और
ज्यादा ताप
पर कराएं, तो
एथेनॉल
का
निर्जलीकरण
होकर
एथीन (C2H4)
बन सकता है।
(viii)
डाइएज़ोनियम लवण
का
सामान्य सूत्र
लिखिए।
उत्तर ✅
Ar–N2+ X− ✅
(जहाँ Ar = एरिल/फिनाइल समूह और X− = Cl−, Br−, HSO4− आदि)
व्याख्या (Step by Step) 👉
डाइएज़ोनियम लवण
में मुख्य आयन होता है
डाइएज़ोनियम आयन
(–N2+)
।
यह आयन प्रायः एरोमैटिक रिंग (Ar) से जुड़ा होता है, इसलिए इसका सामान्य सूत्र लिखा जाता है:
Ar–N2+ X−
उदाहरण:
C6H5N2+Cl− (बेंज़ीन डाइएज़ोनियम क्लोराइड)
क्या आप जानते हैं? 🤔📌
एरोमैटिक डाइएज़ोनियम लवण
(जैसे
बेंज़ीन डाइएज़ोनियम
)
0–5°C
पर ज्यादा स्थिर रहते हैं।
इन्हीं लवणों से Sandmeyer reaction द्वारा Cl/Br/CN जैसे समूह आसानी से रिंग पर लगाए जाते हैं।
(ix)
मेथिलएमीन
से
मेथिलआइसोसायनाइड
में परिवर्तन का
रासायनिक समीकरण
लिखिए।
उत्तर ✅ (रासायनिक समीकरण)
CH3NH2 + CHCl3 + 3KOH (alc.) → CH3NC + 3KCl + 3H2O ✅
व्याख्या (Step by Step) 👉
यह परिवर्तन
कार्बिलअमीन अभिक्रिया (Carbylamine Reaction)
से होता है।
इसमें:
प्राथमिक एमीन (1° amine)
क्लोरोफॉर्म (CHCl3)
और अल्कोहॉलिक KOH
मिलकर आइसोसायनाइड (R–NC) बनाते हैं।
यहाँ R = CH3 होने पर उत्पाद मेथिलआइसोसायनाइड (CH3NC) बनता है।
क्या आप जानते हैं? 🤔📌
कार्बिलअमीन टेस्ट
केवल
प्राथमिक एमीन
के लिए
सकारात्मक
होता है।
बने हुए आइसोसायनाइड (R–NC) की गंध बहुत तीव्र और अप्रिय होती है, इसलिए यह टेस्ट आसानी से पहचान में आ जाता है।
(x)
DNA
तथा
RNA
में कोई एक
अंतर
लिखिए।
उत्तर ✅
DNA में शर्करा “डीऑक्सीराइबोज” होती है, जबकि RNA में शर्करा “राइबोज” होती है। ✅
व्याख्या (Step by Step) 👉
DNA (Deoxyribonucleic acid)
में
राइबोज शर्करा
के
2’ कार्बन
पर
ऑक्सीजन नहीं होती
(इसलिए “डी-ऑक्सी”).
RNA (Ribonucleic acid) में 2’ कार्बन पर –OH समूह होता है।
क्या आप जानते हैं? 🤔📌
DNA
सामान्यतः
द्वि-सूत्री (double stranded)
होता है, जबकि
RNA
अक्सर
एक-सूत्री (single stranded)
होता है।
लघुत्तरात्मक प्रश्न: (उत्तर सीमा लगभग 50 शब्द)
4)
स्थिरक्वाथी
को परिभाषित कीजिए।
न्यूनतम क्वथनांकी स्थिरक्वाथी
को उदाहरण की सहायता से समझाइए।
उत्तर ✅
स्थिरक्वाथी (Azeotrope) की परिभाषा:
“ऐसा द्विघटकीय मिश्रण हैं, जिनका द्रव व वाष्प प्रावस्था में संघटन समान होता है तथा यह एक स्थिर ताप पर उबलते हैं। जिस कारण इन घटकों को प्रभाजी आसवन द्वारा अलग नहीं किया जा सकता।” ✅
📌 न्यूनतम क्वथनांकी स्थिरक्वाथी (Minimum Boiling Azeotrope):
न्यूनतम क्वथनांकी स्थिरक्वाथी वह स्थिरक्वाथी है जिसका
क्वथनांक
उसके दोनों
शुद्ध घटकों
के क्वथनांकों से
कम
होता है।
ऐसा मिश्रण सामान्यतः रॉल्ट के नियम से धनात्मक विचलन दिखाता है।
धनात्मक विचलन में A–B के बीच आकर्षण कमजोर हो जाता है, इसलिए मिश्रण आसानी से वाष्प बनाता है, परिणामस्वरूप क्वथनांक घट जाता है।
✅ उदाहरण (समझिए आसान तरीके से):
एथेनॉल + जल (Ethanol + Water)
एथेनॉल और जल का मिश्रण लगभग
95.6% एथेनॉल + 4.4% जल
पर एक न्यूनतम क्वथनांकी स्थिरक्वाथी बनाता है।
यह मिश्रण लगभग
78.2°C
पर उबलता है, जो मिश्रण के घटकों की तुलना में न्यूनतम/कम माना जाता है।
👉 इसलिए प्रभाजी आसवन से एथेनॉल को 100% शुद्ध करना मुश्किल होता है, क्योंकि स्थिरक्वाथी संरचना पर द्रव और वाष्प का संघटन एक जैसा हो जाता है।
व्याख्या देखें 👉
न्यूनतम क्वथनांकी स्थिरक्वाथी
में
धनात्मक विचलन
की वजह से मिश्रण का
वाष्प दाब
बढ़ता है, इसलिए यह
जल्दी उबलता
है और
क्वथनांक कम
हो जाता है।
क्या आप जानते हैं? 🤔📌
स्थिरक्वाथी बनने पर मिश्रण
“एक ही ताप पर”
उबलता है, इसलिए आसवन में अलग-अलग ताप पर अलग घटक निकलने वाली बात
काम नहीं करती
।
5)
16.0 g NaOH
को जल में घोलकर
800 mL
विलयन बनाया गया। विलयन की
मोलरता
की गणना कीजिए।
उत्तर ✅
विलयन की मोलरता =
0.50 M ✅
व्याख्या (Step-by-step) 👉
मोलरता (M)
=
विलेय के मोल
/
विलयन का आयतन (लीटर में)
1) NaOH के मोल निकालें
NaOH का अणुभार = 23 + 16 + 1 = 40 g mol−1
मोल = द्रव्यमान / अणुभार
मोल = 16.0 / 40 = 0.40 mol
2) आयतन को लीटर में बदलें
800 mL = 0.800 L
3) मोलरता निकालें
M = 0.40 / 0.800 = 0.50 M
क्या आप जानते हैं? 🤔📌
मोलरता
ताप पर निर्भर करती है क्योंकि ताप बदलने पर
विलयन का आयतन
बदल सकता है।
6)
किसी अभिक्रिया के लिए
वेग स्थिरांक (k)
का मान
2.31 × 10−13 s−1
है। अभिक्रिया के लिए
अर्धायु (t1/2)
की गणना कीजिए।
उत्तर ✅
t1/2
=
3.0 × 1012 s (लगभग) ✅
व्याख्या (Step-by-step) 👉
क्योंकि
k
की इकाई
s−1
है, इसलिए यह
प्रथम कोटि (First order)
की अभिक्रिया है।
प्रथम कोटि के लिए अर्धायु का सूत्र:
t1/2 = 0.693 / k
अब मान रखें:
t1/2 = 0.693 / (2.31 × 10−13)
0.693 ÷ 2.31 = 0.300 (लगभग)
तो,
t1/2 ≈ 0.300 × 1013
t1/2 ≈ 3.0 × 1012 s
क्या आप जानते हैं? 🤔📌
प्रथम कोटि
अभिक्रिया की
अर्धायु
प्रारम्भिक
सांद्रता
पर निर्भर नहीं करती।
k जितना छोटा होगा, अभिक्रिया उतनी धीमी होगी और अर्धायु उतनी बड़ी होगी।
7)
द्वितीय एवं तृतीय संक्रमण श्रेणी
(Second & Third Transition Series)
तत्वों की
त्रिज्याएँ
लगभग समान क्यों होती हैं? विश्लेषण कीजिए।
उत्तर ✅
द्वितीय
(4d)
और तृतीय
(5d)
संक्रमण श्रेणी के तत्वों की परमाण्विक/आयनिक त्रिज्याएँ लगभग समान होने का मुख्य कारण
लैंथेनाइड संकुचन (Lanthanide contraction)
है। ✅
व्याख्या (विश्लेषण) 👉
1)
सामान्य नियम क्या कहता है?
सामान्यतः किसी समूह में नीचे जाने पर नई परत जुड़ती है, इसलिए त्रिज्या बढ़नी चाहिए । लेकिन 4d (द्वितीय) से 5d (तृतीय) में जाते समय यह बढ़ोतरी बहुत कम होती है।
2) लैंथेनाइड संकुचन क्या है?
तृतीय संक्रमण श्रेणी (5d) से ठीक पहले लैंथेनाइड श्रृंखला (La से Lu) आती है, जहाँ 4f इलेक्ट्रॉन भरते हैं।
4f इलेक्ट्रॉनों की शील्डिंग क्षमता बहुत कमजोर होती है, यानी ये बाहरी इलेक्ट्रॉनों को नाभिक के आकर्षण से अच्छी तरह नहीं बचा पाते।
3) इसका प्रभाव क्या पड़ता है?
नाभिकीय आवेश (Z) बढ़ता जाता है
लेकिन 4f इलेक्ट्रॉन ठीक से शील्ड नहीं करते
इसलिए बाहरी इलेक्ट्रॉनों पर प्रभावी नाभिकीय आवेश (Zeff) बढ़ जाता है
परिणाम: बाहरी इलेक्ट्रॉन नाभिक की ओर ज्यादा खिंच जाते हैं
➡️ त्रिज्या अपेक्षित बढ़ने की बजाय सिकुड़ जाती है/बहुत कम बढ़ती है
4) अंतिम निष्कर्ष
इसी “संकुचन” की भरपाई के कारण:
5d तत्वों की त्रिज्या असामान्य रूप से छोटी हो जाती है
और वह 4d तत्वों की त्रिज्या के बहुत करीब आ जाती है
उदाहरण (समझने के लिए):
Zr (4d) और Hf (5d) की त्रिज्याएँ बहुत मिलती-जुलती हैं।
इसलिए इनके गुण भी कई बार काफी समान दिखाई देते हैं।
क्या आप जानते हैं? 🤔📌
लैंथेनाइड संकुचन
की वजह से
Zr
और
Hf
को अलग करना
(separation)
काफी मुश्किल होता है क्योंकि उनके गुण बहुत मिलते हैं।
यही कारण है कि तृतीय संक्रमण श्रेणी (5d) के तत्व सामान्यतः बहुत अधिक घनत्व (high density) भी दिखाते हैं।
8)
निम्नलिखित
उपसहसंयोजक (Coordination)
यौगिकों के
IUPAC नाम
लिखिए।
(अ) [Co(NH3)5Cl]Cl2
(ब) K3[Al(C2O4)3]
(अ) [Co(NH3)5Cl]Cl2
(ब) K3[Al(C2O4)3]
उत्तर ✅ (IUPAC नाम)
(अ)
[Co(NH3)5Cl]Cl2
पेंटाऐमाइन क्लोरिडोकोबाल्ट(III) क्लोराइड ✅
(English style: pentaamminechloridocobalt(III) chloride)
(ब) K3[Al(C2O4)3]
पोटैशियम ट्रिस(ऑक्सालेटो)ऐलुमिनेट(III) ✅
(English style: potassium tris(oxalato)aluminate(III))
पेंटाऐमाइन क्लोरिडोकोबाल्ट(III) क्लोराइड ✅
(English style: pentaamminechloridocobalt(III) chloride)
(ब) K3[Al(C2O4)3]
पोटैशियम ट्रिस(ऑक्सालेटो)ऐलुमिनेट(III) ✅
(English style: potassium tris(oxalato)aluminate(III))
व्याख्या (छोटी) 👉
(अ)
बाहर
2Cl−
हैं, इसलिए complex का आवेश
+2
होगा।
NH3 neutral है, अंदर 1 Cl− है ⇒ Co की oxidation state +3 आती है।
(ब) 3K+ होने से complex anion का आवेश −3 है।
हर oxalato (C2O4)2− है, 3 होने पर −6 ⇒ Al की oxidation state +3 आती है।
NH3 neutral है, अंदर 1 Cl− है ⇒ Co की oxidation state +3 आती है।
(ब) 3K+ होने से complex anion का आवेश −3 है।
हर oxalato (C2O4)2− है, 3 होने पर −6 ⇒ Al की oxidation state +3 आती है।
क्या आप जानते हैं? 🤔📌
जब लिगैण्ड का नाम पहले से complex type का हो (जैसे
oxalato
), और संख्या
2 से अधिक
हो, तो
bis/tris
का प्रयोग किया जाता है।
anionic complex में metal के नाम के अंत में “-ate” लगाया जाता है (जैसे aluminate)।
9)
अष्टफलकीय (Octahedral)
क्रिस्टल क्षेत्र में
d-कक्षकों के विभाजन
का नामांकित चित्र
बनाइए।
उत्तर ✅ (चित्र लिंक)
आपका नामांकित चित्र यहाँ है:
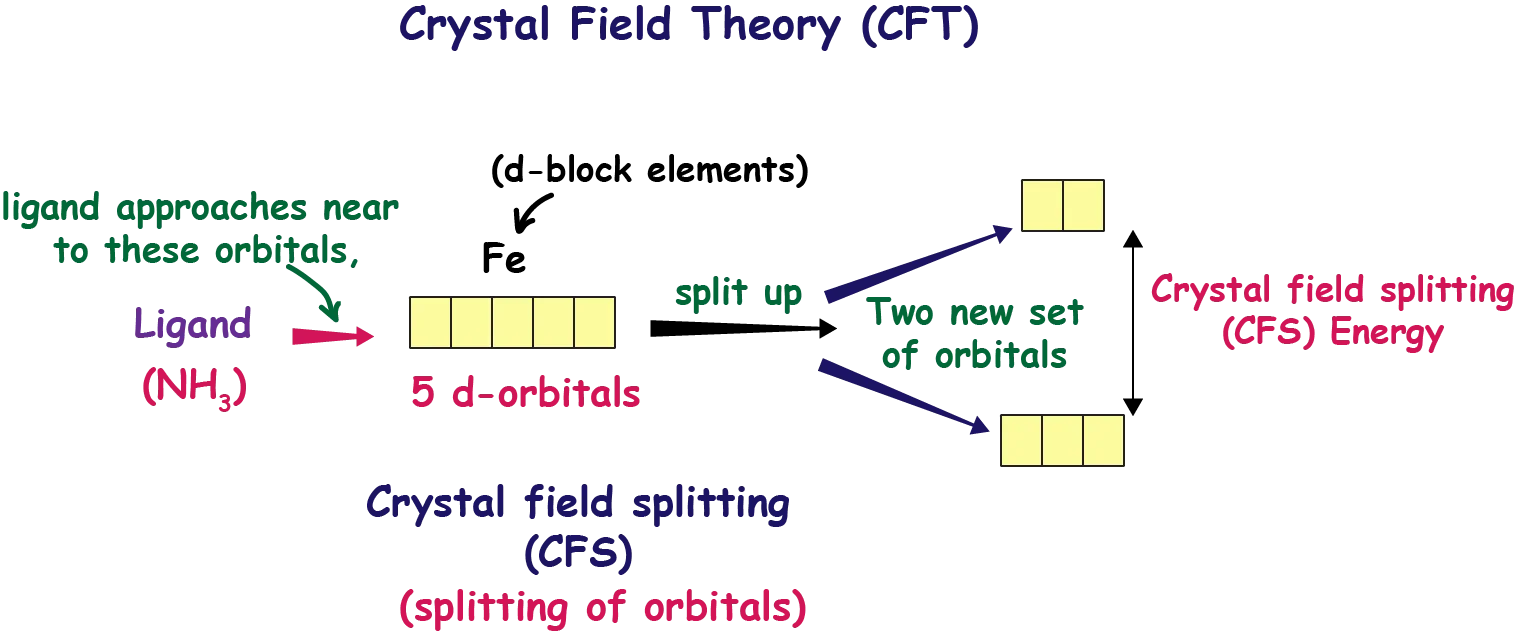
व्याख्या (समझिए आसान भाषा में) 👉
अष्टफलकीय क्रिस्टल क्षेत्र में लिगैंड
6 दिशाओं
से आते हैं, इसलिए
5 d-कक्षक
ऊर्जा के आधार पर
2 समूहों
में बँट जाते हैं:
1) t2g (निम्न ऊर्जा वाले कक्षक)
dxy, dyz, dxz
ये अक्षों (axes) के बीच में होते हैं, इसलिए लिगैंड से प्रतिकर्षण कम होता है → ऊर्जा कम।
2) eg (उच्च ऊर्जा वाले कक्षक)
dx²−y², dz²
ये सीधे अक्षों पर होते हैं, जहाँ लिगैंड आते हैं → प्रतिकर्षण ज्यादा → ऊर्जा ज्यादा।
🔹 ऊर्जा अंतर
इन दोनों समूहों के बीच ऊर्जा के अंतर को Δo (डेल्टा-ओ) या 10Dq कहते हैं।
क्या आप जानते हैं? 🤔📌
Δo
जितना बड़ा, इलेक्ट्रॉन
pairing
की संभावना उतनी ज्यादा होती है और
low spin complex
बनने की संभावना बढ़ती है।
CN−, CO जैसे strong field ligands अक्सर Δo बड़ा करते हैं, जबकि F−, H2O जैसे ligands में Δo छोटा रहता है।
10)
एल्डिहाइड
नाभिकरागी योजक अभिक्रियाओं
के प्रति
कीटोन
से अधिक क्रियाशील क्यों होते हैं? समझाइए।
उत्तर ✅
एल्डिहाइड (R–CHO) कीटोन (R–CO–R’) की तुलना में नाभिकरागी योजक अभिक्रियाओं के प्रति अधिक क्रियाशील होते हैं, क्योंकि एल्डिहाइड में इलेक्ट्रॉन दान करने वाले अल्किल समूह कम होते हैं और त्रिविम बाधा (steric hindrance) भी कम होती है।
व्याख्या (मुख्य कारण) 👉
1)
+I प्रभाव
कम होने से
कार्बोनिल कार्बन
ज्यादा
धनात्मक
होता है
एल्डिहाइड में कार्बोनिल के साथ एक अल्किल समूह + एक H होता है।
कीटोन में दो अल्किल समूह होते हैं।
अल्किल समूह +I प्रभाव से इलेक्ट्रॉन धकेलते हैं, जिससे कार्बोनिल कार्बन पर δ+ कम हो जाता है।
👉 इसलिए कीटोन में कार्बोनिल कार्बन कम इलेक्ट्रोफिलिक होता है और नाभिकरागी आक्रमण धीमा हो जाता है।
👉 एल्डिहाइड में यह प्रभाव कम होता है, इसलिए नाभिकरागी आसानी से जुड़ता है।
2) त्रिविम बाधा (Steric Hindrance) कम
एल्डिहाइड में कार्बोनिल कार्बन के पास एक ही अल्किल समूह होता है, जगह खुली रहती है।
कीटोन में दो अल्किल समूह होने से आसपास भीड़ बढ़ जाती है।
👉 नाभिकरागी का पास आना कठिन → अभिक्रिया धीमी ।
क्या आप जानते हैं? 🤔📌
सामान्य क्रियाशीलता क्रम (नाभिकरागी योजक के लिए):
HCHO (फॉर्मेल्डिहाइड) > RCHO (एल्डिहाइड) > R2CO (कीटोन)
फॉर्मेल्डिहाइड सबसे अधिक क्रियाशील होता है क्योंकि इसमें दोनों तरफ H होते हैं (ना +I, ना steric hindrance )।
11)
निम्नलिखित यौगिकों के
संरचनात्मक सूत्र
लिखिए।
(अ) सक्सीनिक अम्ल
(ब) थैलिक अम्ल
(अ) सक्सीनिक अम्ल
(ब) थैलिक अम्ल
उत्तर ✅
(अ)
सक्सीनिक अम्ल (Succinic acid)
संरचनात्मक सूत्र: HOOC–CH2–CH2–COOH
(अर्थात: ब्यूटेन-1,4-डाइओइक अम्ल)
(ब) थैलिक अम्ल (Phthalic acid)
संरचनात्मक सूत्र: o-C6H4(COOH)2
(बेंजीन रिंग पर पड़ोसी (ortho) स्थान पर दो –COOH)
सरल लिखावट में: HOOC–C6H4–COOH (ortho)
(अर्थात: बेंजीन-1,2-डाइकार्बोक्सिलिक अम्ल)
संरचनात्मक सूत्र: HOOC–CH2–CH2–COOH
(अर्थात: ब्यूटेन-1,4-डाइओइक अम्ल)
(ब) थैलिक अम्ल (Phthalic acid)
संरचनात्मक सूत्र: o-C6H4(COOH)2
(बेंजीन रिंग पर पड़ोसी (ortho) स्थान पर दो –COOH)
सरल लिखावट में: HOOC–C6H4–COOH (ortho)
(अर्थात: बेंजीन-1,2-डाइकार्बोक्सिलिक अम्ल)
व्याख्या देखें 👉
सक्सीनिक अम्ल
में दो
–COOH
समूह
सीधी श्रृंखला
के दोनों सिरों पर होते हैं, जबकि
थैलिक अम्ल
में दो
–COOH
समूह
बेंजीन रिंग
पर
ortho (1,2)
स्थिति में होते हैं।
क्या आप जानते हैं? 🤔📌
थैलिक अम्ल
के
3 समावयवी
होते हैं:
ओर्थो (phthalic),
मेटा (isophthalic),
पेरा (terephthalic)
— फर्क सिर्फ
–COOH
की स्थिति का होता है।
12)
ऐनिलीन (C6H5NH2)
की
अनुनादी (resonance) संरचनाएँ
बनाइए।
उत्तर ✅
ऐनिलीन में
–NH2
समूह का
लोन पेयर (:)
बेंजीन रिंग के
π-तंत्र
में दान करता है। इसलिए रिंग पर
ओर्थो (o)
और
पेरा (p)
स्थानों पर इलेक्ट्रॉन घनत्व बढ़ता है और अनुनाद संरचनाएँ बनती हैं।
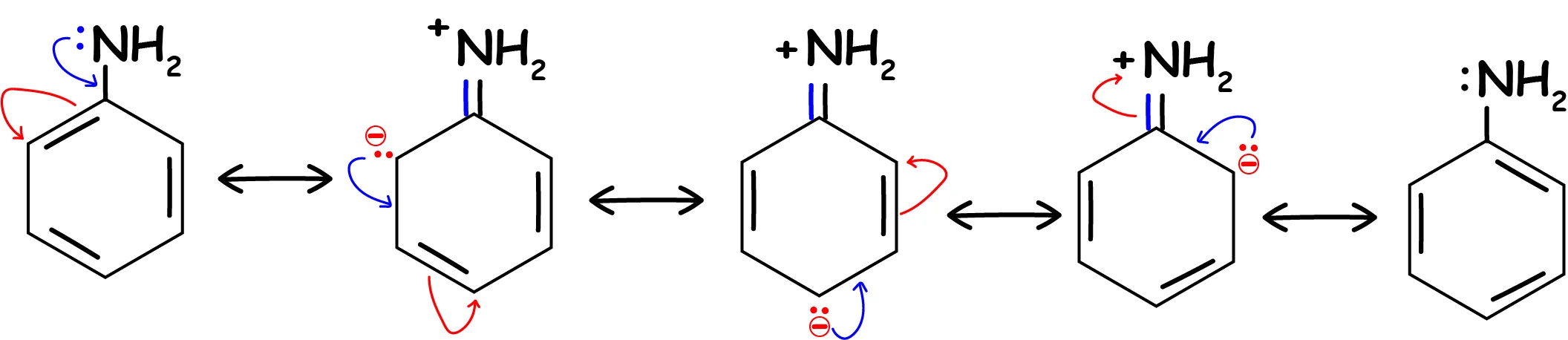
Explanation: 📌 अनुनादी संरचनाएँ :
(1) मूल संरचना (Neutral form):
C6H5–NH2 (N पर lone pair : )
(2) ओर्थो-कार्बन पर ऋण आवेश वाला रूप (o-form):
N का lone pair रिंग में गया ⇒ N पर + और ओर्थो कार्बन पर −
C6H4(o−)–NH2+
(3) पेरा-कार्बन पर ऋण आवेश वाला रूप (p-form):
C6H4(p−)–NH2+
(4) दूसरे ओर्थो-कार्बन पर ऋण आवेश वाला रूप (o′-form):
C6H4(o′−)–NH2+
(इनके साथ रिंग के डबल बांड भी शिफ्ट होते हैं, यही अनुनाद है।)
व्याख्या देखें 👉
अनुनाद में
लोन पेयर
का दान होने से रिंग पर
o/p
स्थानों पर
इलेक्ट्रॉन घनत्व
बढ़ता है, इसलिए ये स्थान अभिक्रियाओं में अधिक सक्रिय हो जाते हैं।
क्या आप जानते हैं? 🤔📌
इसी अनुनाद
(lone pair donation)
की वजह से
–NH2
समूह रिंग को
सक्रिय
करता है और इलेक्ट्रोफिलिक प्रतिस्थापन में मुख्यतः
ओर्थो
और
पेरा
निर्देशित (o/p directing) होता है।
13)
प्रोटीन
के
विकृतिकरण (Denaturation)
को समझाइए।
उत्तर ✅
प्रोटीन का विकृतिकरण वह प्रक्रिया है जिसमें प्रोटीन की प्राकृतिक त्रिविम (3D) संरचना बिगड़ जाती है, जिससे उसका जैविक कार्य (biological activity) समाप्त या बहुत कम हो जाता है।
व्याख्या 👉
प्रोटीन की
प्राथमिक संरचना
(अमीनो अम्लों का क्रम) आमतौर पर नहीं टूटती, क्योंकि इसमें
पेप्टाइड बंध
होते हैं।
लेकिन द्वितीयक (α-helix, β-sheet) और तृतीयक/चतुर्थक संरचना टूट जाती है।
यह टूटना मुख्यतः इन बंधों के टूटने से होता है:
हाइड्रोजन बंध
आयनिक बंध
हाइड्रोफोबिक आकर्षण
कभी-कभी डाइसल्फाइड बंध भी प्रभावित हो सकते हैं।
✅ विकृतिकरण के कारण (कुछ सामान्य)
ताप बढ़ाना (Heating)
अम्ल/क्षार (pH बदलना)
अल्कोहल, यूरिया, डिटर्जेंट जैसे रसायन
भारी धातु आयन (Hg²⁺, Pb²⁺ आदि)
क्या आप जानते हैं? 🤔📌
अंडे का सफेद भाग
पकने पर जो जम जाता है, वह प्रोटीन
(एल्ब्यूमिन)
के विकृतिकरण का ही उदाहरण है।
विकृतिकरण के बाद प्रोटीन अक्सर पानी में कम घुलनशील हो जाता है और जम (coagulate) सकता है।
दीर्घत्तरात्मक प्रश्न: (उत्तर सीमा लगभग 100 शब्द)
14)
(अ) अभिक्रिया की कोटि (Order) एवं आण्विकता (Molecularity) में कोई दो अंतर लिखिए।
(ब) शून्य कोटि (Zero order) अभिक्रिया के लिए समाकलित वेग समीकरण का व्यंजक व्युत्पन्न कीजिए।
(अ) अभिक्रिया की कोटि (Order) एवं आण्विकता (Molecularity) में कोई दो अंतर लिखिए।
(ब) शून्य कोटि (Zero order) अभिक्रिया के लिए समाकलित वेग समीकरण का व्यंजक व्युत्पन्न कीजिए।
उत्तर ✅
(अ)
✅ कोटि एवं आण्विकता में दो अंतर
1) अर्थ / परिभाषा
कोटि (Order): वेग नियम (Rate law) में अभिकारकों की सांद्रता के घातांकों का योग।
आण्विकता (Molecularity): किसी प्राथमिक (elementary) चरण में टकराने वाले कणों (अणु/आयन) की संख्या।
2) निर्धारण कैसे होता है?
कोटि: हमेशा प्रयोग (experiment) से ज्ञात होती है।
आण्विकता: अभिक्रिया के तंत्र/प्राथमिक चरण से तय होती है (प्रयोग से सीधे नहीं निकलती) ।
(छोटा अतिरिक्त याद रखने लायक: कोटि शून्य/भिन्नात्मक भी हो सकती है, लेकिन आण्विकता हमेशा 1, 2, 3… ही होती है।)
(ब) ✅ शून्य कोटि अभिक्रिया का समाकलित वेग समीकरण (व्युत्पत्ति)
मान लीजिए अभिक्रिया: A → उत्पाद
1) शून्य कोटि के लिए वेग नियम
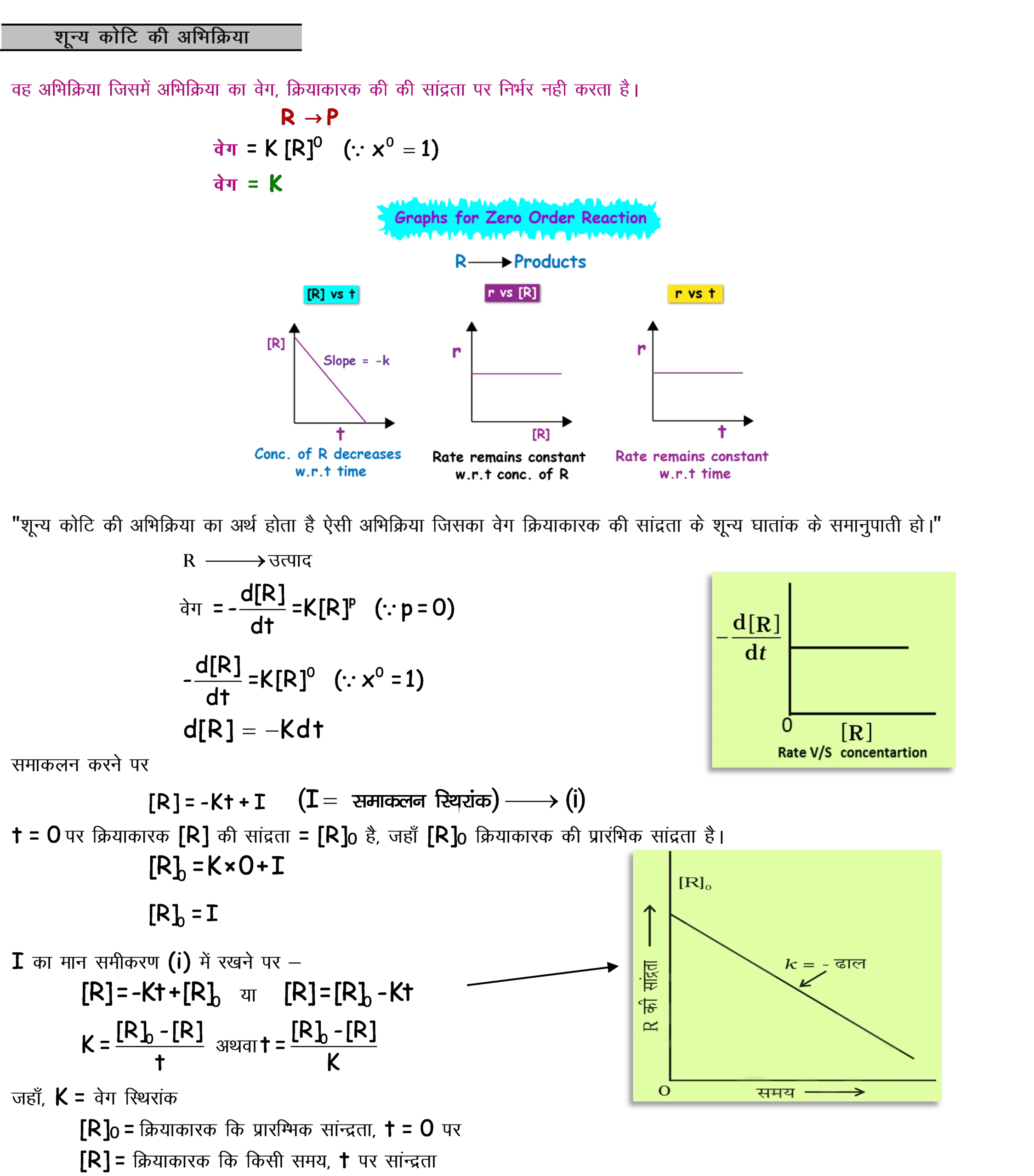
1) अर्थ / परिभाषा
कोटि (Order): वेग नियम (Rate law) में अभिकारकों की सांद्रता के घातांकों का योग।
आण्विकता (Molecularity): किसी प्राथमिक (elementary) चरण में टकराने वाले कणों (अणु/आयन) की संख्या।
2) निर्धारण कैसे होता है?
कोटि: हमेशा प्रयोग (experiment) से ज्ञात होती है।
आण्विकता: अभिक्रिया के तंत्र/प्राथमिक चरण से तय होती है (प्रयोग से सीधे नहीं निकलती) ।
(छोटा अतिरिक्त याद रखने लायक: कोटि शून्य/भिन्नात्मक भी हो सकती है, लेकिन आण्विकता हमेशा 1, 2, 3… ही होती है।)
(ब) ✅ शून्य कोटि अभिक्रिया का समाकलित वेग समीकरण (व्युत्पत्ति)
मान लीजिए अभिक्रिया: A → उत्पाद
1) शून्य कोटि के लिए वेग नियम

व्याख्या देखें 👉
शून्य कोटि में
वेग
सांद्रता पर निर्भर नहीं
करता, इसलिए समय के साथ
[A]
रैखिक रूप से घटती है।
क्या आप जानते हैं? 🤔📌
शून्य कोटि अभिक्रिया में
[A] v/s t
का ग्राफ
सीधी रेखा
देता है और उसका ढाल
−k
होता है।
शून्य कोटि की अर्धायु: t1/2 = [A]0 / (2k)
अथवा
14)
(अ) अभिक्रिया के औसत वेग एवं तात्क्षणिक वेग में भेद कीजिए।
(ब) प्रथम कोटि अभिक्रिया के लिए समाकलित वेग समीकरण का व्यंजक व्युत्पन्न कीजिए।
(अ) अभिक्रिया के औसत वेग एवं तात्क्षणिक वेग में भेद कीजिए।
(ब) प्रथम कोटि अभिक्रिया के लिए समाकलित वेग समीकरण का व्यंजक व्युत्पन्न कीजिए।
उत्तर ✅
(अ)
✅ औसत वेग और तात्क्षणिक वेग में भेद
1) परिभाषा
औसत वेग (Average rate): किसी समयांतराल (Δt) में सांद्रता में हुए परिवर्तन के आधार पर वेग।
- उदाहरण: −Δ[A]/Δt
तात्क्षणिक वेग (Instantaneous rate): किसी विशेष क्षण (exact time) पर वेग।
- उदाहरण: −d[A]/dt
2) निर्भरता/प्रकृति
औसत वेग: समयांतराल चुनने पर बदल सकता है, इसलिए यह लगभग मान देता है।
तात्क्षणिक वेग: उसी क्षण का वास्तविक वेग बताता है, यह अधिक सटीक होता है (ग्राफ पर tangent से मिलता है) ।
(ब) ✅ प्रथम कोटि अभिक्रिया का समाकलित वेग समीकरण (व्युत्पत्ति)
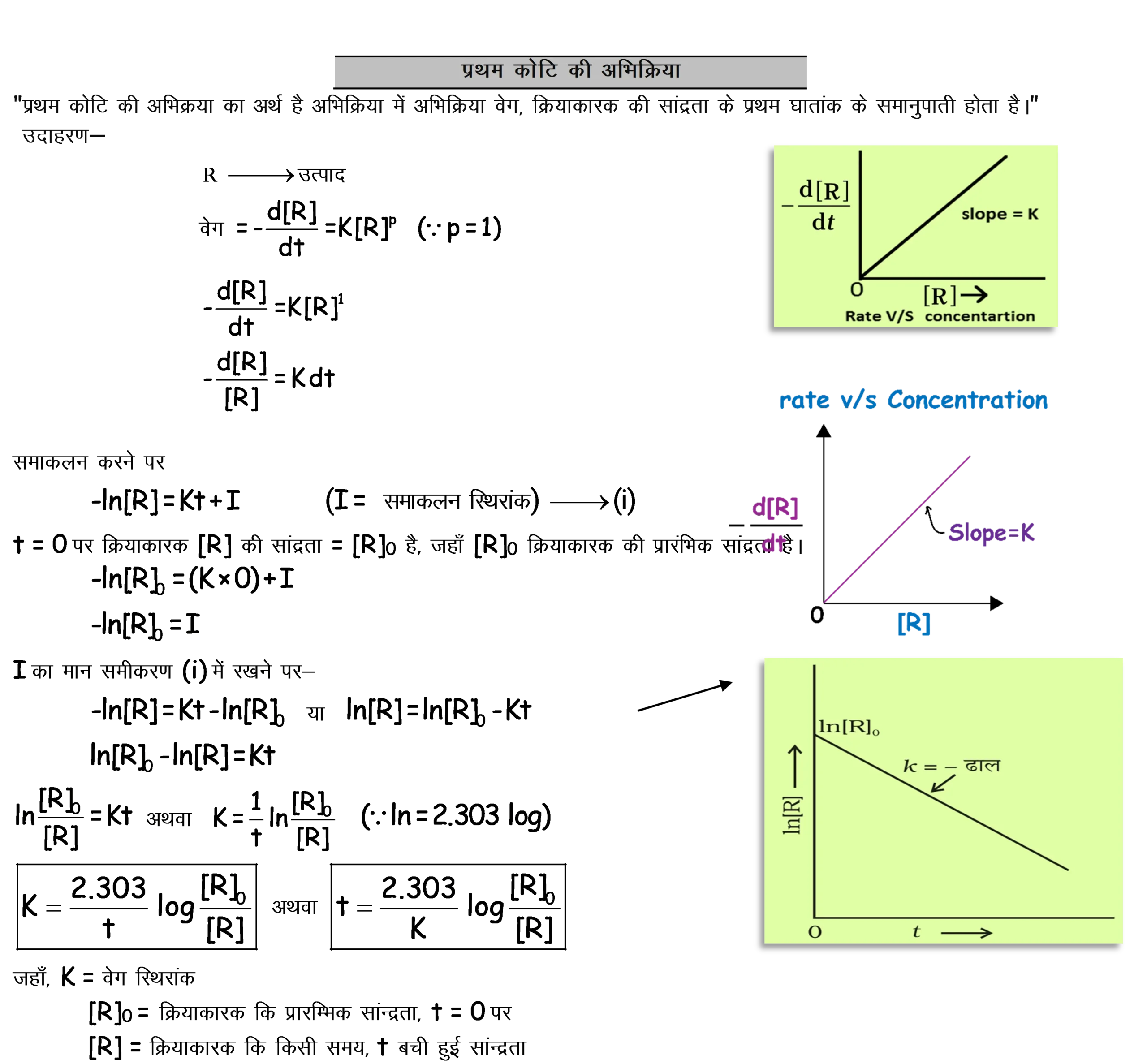
1) परिभाषा
औसत वेग (Average rate): किसी समयांतराल (Δt) में सांद्रता में हुए परिवर्तन के आधार पर वेग।
- उदाहरण: −Δ[A]/Δt
तात्क्षणिक वेग (Instantaneous rate): किसी विशेष क्षण (exact time) पर वेग।
- उदाहरण: −d[A]/dt
2) निर्भरता/प्रकृति
औसत वेग: समयांतराल चुनने पर बदल सकता है, इसलिए यह लगभग मान देता है।
तात्क्षणिक वेग: उसी क्षण का वास्तविक वेग बताता है, यह अधिक सटीक होता है (ग्राफ पर tangent से मिलता है) ।
(ब) ✅ प्रथम कोटि अभिक्रिया का समाकलित वेग समीकरण (व्युत्पत्ति)

व्याख्या देखें 👉
प्रथम कोटि में
वेग
[A]
के समानुपाती होता है, इसलिए समाकलन करने पर
log
वाला रूप मिलता है।
क्या आप जानते हैं? 🤔📌
प्रथम कोटि अभिक्रिया की अर्धायु:
t1/2 = 0.693 / k
इसकी अर्धायु प्रारम्भिक सांद्रता पर निर्भर नहीं करती।
15)
(अ) फिंकेलस्टाइन अभिक्रिया का रासायनिक समीकरण लिखिए।
(ब) हैलोऐल्केन की KCN तथा AgCN से अभिक्रिया से प्राप्त मुख्य उत्पादों की तुलना कीजिए।
(अ) फिंकेलस्टाइन अभिक्रिया का रासायनिक समीकरण लिखिए।
(ब) हैलोऐल्केन की KCN तथा AgCN से अभिक्रिया से प्राप्त मुख्य उत्पादों की तुलना कीजिए।
उत्तर ✅
(अ)
✅ फिंकेलस्टाइन अभिक्रिया (Finkelstein Reaction) का समीकरण
यह हैलोऐल्केन का आयोडोऐल्केन में परिवर्तन है (आमतौर पर एसीटोन में):
R–Cl / R–Br + NaI (acetone) → R–I + NaCl / NaBr↓
(यहाँ NaCl या NaBr एसीटोन में कम घुलनशील होने से अवक्षेप बनाकर अभिक्रिया आगे बढ़ा देता है।)
(ब) ✅ KCN और AgCN से अभिक्रिया: मुख्य उत्पादों की तुलना
1) KCN के साथ (मुख्य उत्पाद: नाइट्राइल )
R–X + KCN → R–C≡N + KX
मुख्य उत्पाद: अल्किल सायनाइड / नाइट्राइल (R–CN)
कारण: KCN आयनिक होता है, CN− में कार्बन (C) वाला सिरा ज्यादा नाभिकरागी होता है, इसलिए C से जुड़कर R–CN बनता है।
2) AgCN के साथ (मुख्य उत्पाद: आइसोसायनाइड )
R–X + AgCN → R–N≡C + AgX↓
मुख्य उत्पाद: अल्किल आइसोसायनाइड (R–NC)
कारण: AgCN अधिक सहसंयोजक प्रकृति का होता है; यहाँ जुड़ाव अक्सर नाइट्रोजन (N) वाले सिरे से होता है, इसलिए R–NC बनता है।
✅ एक लाइन में तुलना
KCN → R–CN (नाइट्राइल) मुख्य
AgCN → R–NC (आइसोसायनाइड) मुख्य
यह हैलोऐल्केन का आयोडोऐल्केन में परिवर्तन है (आमतौर पर एसीटोन में):
R–Cl / R–Br + NaI (acetone) → R–I + NaCl / NaBr↓
(यहाँ NaCl या NaBr एसीटोन में कम घुलनशील होने से अवक्षेप बनाकर अभिक्रिया आगे बढ़ा देता है।)
(ब) ✅ KCN और AgCN से अभिक्रिया: मुख्य उत्पादों की तुलना
1) KCN के साथ (मुख्य उत्पाद: नाइट्राइल )
R–X + KCN → R–C≡N + KX
मुख्य उत्पाद: अल्किल सायनाइड / नाइट्राइल (R–CN)
कारण: KCN आयनिक होता है, CN− में कार्बन (C) वाला सिरा ज्यादा नाभिकरागी होता है, इसलिए C से जुड़कर R–CN बनता है।
2) AgCN के साथ (मुख्य उत्पाद: आइसोसायनाइड )
R–X + AgCN → R–N≡C + AgX↓
मुख्य उत्पाद: अल्किल आइसोसायनाइड (R–NC)
कारण: AgCN अधिक सहसंयोजक प्रकृति का होता है; यहाँ जुड़ाव अक्सर नाइट्रोजन (N) वाले सिरे से होता है, इसलिए R–NC बनता है।
✅ एक लाइन में तुलना
KCN → R–CN (नाइट्राइल) मुख्य
AgCN → R–NC (आइसोसायनाइड) मुख्य
व्याख्या देखें 👉
KCN
आयनिक होने से
CN−
का
C-end
अधिक nucleophilic होता है, जबकि
AgCN
की सहसंयोजक प्रकृति में जुड़ाव
N-end
से अधिक होता है।
क्या आप जानते हैं? 🤔📌
R–CN
में कार्बन चेन में
1 कार्बन बढ़
जाता है (क्योंकि CN जुड़ता है)।
R–NC (आइसोसायनाइड) की गंध अक्सर बहुत तीव्र/अप्रिय होती है।
अथवा
15) (अ)
वुर्ट्ज अभिक्रिया
का
रासायनिक समीकरण
लिखिए।
(ब) ऐल्किल हैलाइडों की तुलना में ऐरिल हैलाइड नाभिकरागी प्रतिस्थापन अभिक्रियाओं के प्रति कम क्रियाशील क्यों होते हैं? विश्लेषण कीजिए।
(ब) ऐल्किल हैलाइडों की तुलना में ऐरिल हैलाइड नाभिकरागी प्रतिस्थापन अभिक्रियाओं के प्रति कम क्रियाशील क्यों होते हैं? विश्लेषण कीजिए।
उत्तर ✅
(अ)
✅ वुर्ट्ज (Wurtz) अभिक्रिया का समीकरण
2R–X + 2Na —(शुष्क ईथर)→ R–R + 2NaX
जहाँ R = ऐल्किल समूह, X = Cl/Br/I
(यह अभिक्रिया दो ऐल्किल हैलाइडों को जोड़कर उच्च ऐल्केन बनाती है।)
(ब) ✅ ऐरिल हैलाइड नाभिकरागी प्रतिस्थापन के प्रति कम क्रियाशील क्यों?
1) C–X बंध का आंशिक द्विबंध चरित्र (resonance)
ऐरिल हैलाइड (जैसे C6H5Cl ) में हैलोजन का lone pair रिंग के साथ अनुनाद में आ जाता है।
इससे C–X बंध में आंशिक द्विबंध (partial double bond) बन जाता है।
👉 बंध छोटा और मजबूत हो जाता है, इसलिए टूटना कठिन → अभिक्रिया धीमी।
2) sp2 कार्बन पर बंध होने से बंध मजबूत
ऐरिल हैलाइड में हैलोजन sp2 कार्बन से जुड़ा होता है।
sp2 में s-चरित्र ज्यादा होने से C–X बंध अधिक मजबूत होता है।
👉 इसलिए प्रतिस्थापन कठिन।
3) SN1 संभव नहीं (अस्थिर एरिल कार्बोकैटायन)
SN1 में कार्बोकैटायन बनता है, लेकिन C6H5+ (aryl carbocation) बहुत अस्थिर होता है।
👉 इसलिए SN1 मार्ग नहीं चलता।
4) SN2 भी मुश्किल (Backside attack नहीं हो पाता)
SN2 के लिए पीछे से हमला जरूरी होता है, लेकिन ऐरिल हैलाइड में:
रिंग समतलीय (planar) होती है
C–X बंध के पीछे इलेक्ट्रॉन घनत्व/रचना ऐसी होती है कि backside attack बाधित होता है
👉 SN2 भी बहुत कठिन।
2R–X + 2Na —(शुष्क ईथर)→ R–R + 2NaX
जहाँ R = ऐल्किल समूह, X = Cl/Br/I
(यह अभिक्रिया दो ऐल्किल हैलाइडों को जोड़कर उच्च ऐल्केन बनाती है।)
(ब) ✅ ऐरिल हैलाइड नाभिकरागी प्रतिस्थापन के प्रति कम क्रियाशील क्यों?
1) C–X बंध का आंशिक द्विबंध चरित्र (resonance)
ऐरिल हैलाइड (जैसे C6H5Cl ) में हैलोजन का lone pair रिंग के साथ अनुनाद में आ जाता है।
इससे C–X बंध में आंशिक द्विबंध (partial double bond) बन जाता है।
👉 बंध छोटा और मजबूत हो जाता है, इसलिए टूटना कठिन → अभिक्रिया धीमी।
2) sp2 कार्बन पर बंध होने से बंध मजबूत
ऐरिल हैलाइड में हैलोजन sp2 कार्बन से जुड़ा होता है।
sp2 में s-चरित्र ज्यादा होने से C–X बंध अधिक मजबूत होता है।
👉 इसलिए प्रतिस्थापन कठिन।
3) SN1 संभव नहीं (अस्थिर एरिल कार्बोकैटायन)
SN1 में कार्बोकैटायन बनता है, लेकिन C6H5+ (aryl carbocation) बहुत अस्थिर होता है।
👉 इसलिए SN1 मार्ग नहीं चलता।
4) SN2 भी मुश्किल (Backside attack नहीं हो पाता)
SN2 के लिए पीछे से हमला जरूरी होता है, लेकिन ऐरिल हैलाइड में:
रिंग समतलीय (planar) होती है
C–X बंध के पीछे इलेक्ट्रॉन घनत्व/रचना ऐसी होती है कि backside attack बाधित होता है
👉 SN2 भी बहुत कठिन।
व्याख्या देखें 👉
ऐरिल हैलाइड में
resonance
के कारण
C–X बंध मजबूत
हो जाता है और
SN1/SN2
दोनों रास्ते आसानी से नहीं चलते, इसलिए ये अल्किल हैलाइड की तुलना में कम क्रियाशील होते हैं।
क्या आप जानते हैं? 🤔📌
अगर बेंजीन रिंग पर
−NO2
जैसे
strong electron withdrawing group
(o/p पर) लगे हों, तो ऐरिल हैलाइड
SNAr (nucleophilic aromatic substitution)
से प्रतिक्रिया कर सकते हैं (जैसे
p-nitrochlorobenzene
)।
16)
(अ) वैनिला सेम से प्राप्त ऐल्डिहाइड का नाम लिखिए।
(ब) निम्नलिखित रासायनिक समीकरणों को पूर्ण कीजिए एवं मुख्य उत्पाद लिखिए।
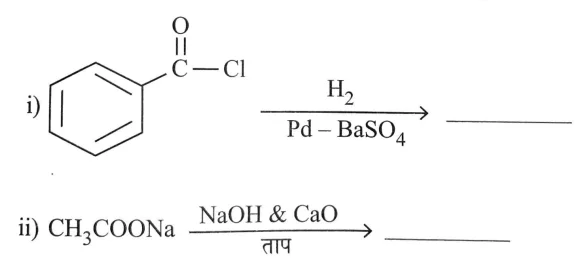
(अ) वैनिला सेम से प्राप्त ऐल्डिहाइड का नाम लिखिए।
(ब) निम्नलिखित रासायनिक समीकरणों को पूर्ण कीजिए एवं मुख्य उत्पाद लिखिए।

उत्तर ✅
(अ)
✅ उत्तर
वैनिलिन (Vanillin) ✅
(ब) ✅ समीकरण पूर्ण कीजिए + मुख्य उत्पाद
(i)
C6H5COCl + H2 —(Pd–BaSO4)→ C6H5CHO
✅ मुख्य उत्पाद: बेंजैल्डिहाइड (Benzaldehyde)
(ii)
CH3COONa + NaOH —(CaO, ताप)→ CH4 + Na2CO3
✅ मुख्य उत्पाद: मीथेन (CH4)
वैनिलिन (Vanillin) ✅
(ब) ✅ समीकरण पूर्ण कीजिए + मुख्य उत्पाद
(i)
C6H5COCl + H2 —(Pd–BaSO4)→ C6H5CHO
✅ मुख्य उत्पाद: बेंजैल्डिहाइड (Benzaldehyde)
(ii)
CH3COONa + NaOH —(CaO, ताप)→ CH4 + Na2CO3
✅ मुख्य उत्पाद: मीथेन (CH4)
व्याख्या ✅
(अ)
📌 व्याख्या
वैनिला सेम की खास खुशबू का मुख्य कारण वैनिलिन होता है। यह एक सुगंधित (aromatic) ऐल्डिहाइड है, इसलिए इसे “वैनिला सेम से प्राप्त ऐल्डिहाइड” कहा जाता है।
(ब) ✅ समीकरण पूर्ण कीजिए + मुख्य उत्पाद + व्याख्या
(i)
📌 व्याख्या
यह अभिक्रिया रोसेनमुण्ड अपचयन (Rosenmund reduction) है।
यहाँ ऐसिल क्लोराइड (C6H5COCl) को हाइड्रोजन (H2) से अपचयित ऐल्डिहाइड (C6H5CHO) बनाया जाता है।
Pd–BaSO4 “poisoned catalyst” की तरह काम करता है, यानी अभिक्रिया को सिर्फ ऐल्डिहाइड तक रोक देता है।
👉 इसलिए उत्पाद ऐल्डिहाइड पर ही रुकता है, आगे अल्कोहॉल नहीं बनता।
(ii)
📌 व्याख्या
यह सोडा लाइम (NaOH + CaO) द्वारा डीकार्बॉक्सिलेशन है।
सोडियम एसीटेट (CH3COONa) से –COO⁻ समूह निकल जाता है (CO2 हटता है)
और एक कार्बन कम वाला ऐल्केन बनता है। यहाँ एसीटेट में 2 कार्बन थे, इसलिए उत्पाद 1 कार्बन वाला ऐल्केन = CH4 बनता है।
वैनिला सेम की खास खुशबू का मुख्य कारण वैनिलिन होता है। यह एक सुगंधित (aromatic) ऐल्डिहाइड है, इसलिए इसे “वैनिला सेम से प्राप्त ऐल्डिहाइड” कहा जाता है।
(ब) ✅ समीकरण पूर्ण कीजिए + मुख्य उत्पाद + व्याख्या
(i)
📌 व्याख्या
यह अभिक्रिया रोसेनमुण्ड अपचयन (Rosenmund reduction) है।
यहाँ ऐसिल क्लोराइड (C6H5COCl) को हाइड्रोजन (H2) से अपचयित ऐल्डिहाइड (C6H5CHO) बनाया जाता है।
Pd–BaSO4 “poisoned catalyst” की तरह काम करता है, यानी अभिक्रिया को सिर्फ ऐल्डिहाइड तक रोक देता है।
👉 इसलिए उत्पाद ऐल्डिहाइड पर ही रुकता है, आगे अल्कोहॉल नहीं बनता।
(ii)
📌 व्याख्या
यह सोडा लाइम (NaOH + CaO) द्वारा डीकार्बॉक्सिलेशन है।
सोडियम एसीटेट (CH3COONa) से –COO⁻ समूह निकल जाता है (CO2 हटता है)
और एक कार्बन कम वाला ऐल्केन बनता है। यहाँ एसीटेट में 2 कार्बन थे, इसलिए उत्पाद 1 कार्बन वाला ऐल्केन = CH4 बनता है।
क्या आप जानते हैं? 🤔📌
वैनिलिन
का संरचनात्मक नाम:
4-हाइड्रॉक्सी-3-मेथॉक्सीबेंजैल्डिहाइड
(यही वैनिला की signature smell देता है)।
अगर बहुत strong catalyst/conditions हों, तो ऐसिल क्लोराइड आगे घटकर अल्कोहॉल भी बन सकता है, लेकिन Pd–BaSO4 इसे रोक देता है।
सोडा लाइम डीकार्बॉक्सिलेशन का नियम: R–COONa → R–H (यानी एक कार्बन कम)
अगर बहुत strong catalyst/conditions हों, तो ऐसिल क्लोराइड आगे घटकर अल्कोहॉल भी बन सकता है, लेकिन Pd–BaSO4 इसे रोक देता है।
सोडा लाइम डीकार्बॉक्सिलेशन का नियम: R–COONa → R–H (यानी एक कार्बन कम)
अथवा
16)
(अ) मेडोस्वीट (Meadowsweet) से प्राप्त ऐल्डिहाइड का नाम लिखिए।
(ब) निम्नलिखित रासायनिक समीकरणों को पूर्ण कीजिए एवं मुख्य उत्पाद लिखिए।
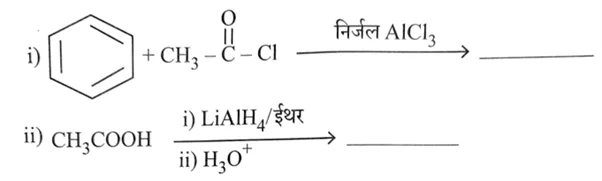
(अ) मेडोस्वीट (Meadowsweet) से प्राप्त ऐल्डिहाइड का नाम लिखिए।
(ब) निम्नलिखित रासायनिक समीकरणों को पूर्ण कीजिए एवं मुख्य उत्पाद लिखिए।

उत्तर ✅
(अ)
✅ उत्तर
सैलिसिलऐल्डिहाइड (Salicylaldehyde) ✅
(इसे 2-हाइड्रॉक्सीबेंजैल्डिहाइड भी कहते हैं)
(ब) ✅ समीकरण पूर्ण कीजिए + मुख्य उत्पाद
(i) बेंजीन + एसीटिल क्लोराइड (निर्जल AlCl3)
C6H6 + CH3COCl —(निर्जल AlCl3)→ C6H5COCH3 + HCl
✅ मुख्य उत्पाद: एसीटोफिनोन (Acetophenone) ✅
(ii) CH3COOH का LiAlH4 से अपचयन
CH3COOH —(1) LiAlH4/ईथर (2) H3O+→ CH3CH2OH
✅ मुख्य उत्पाद: एथेनॉल (Ethanol) ✅
सैलिसिलऐल्डिहाइड (Salicylaldehyde) ✅
(इसे 2-हाइड्रॉक्सीबेंजैल्डिहाइड भी कहते हैं)
(ब) ✅ समीकरण पूर्ण कीजिए + मुख्य उत्पाद
(i) बेंजीन + एसीटिल क्लोराइड (निर्जल AlCl3)
C6H6 + CH3COCl —(निर्जल AlCl3)→ C6H5COCH3 + HCl
✅ मुख्य उत्पाद: एसीटोफिनोन (Acetophenone) ✅
(ii) CH3COOH का LiAlH4 से अपचयन
CH3COOH —(1) LiAlH4/ईथर (2) H3O+→ CH3CH2OH
✅ मुख्य उत्पाद: एथेनॉल (Ethanol) ✅
व्याख्या ✅
(अ)
📌 व्याख्या
मेडोस्वीट पौधे से संबंधित सुगंधित यौगिकों में सैलिसिलऐल्डिहाइड पाया जाता है, इसलिए इसे “मेडोस्वीट से प्राप्त ऐल्डिहाइड” के रूप में पूछा जाता है।
(ब) ✅ व्याख्या
(i) यह फ्राइडेल–क्राफ्ट्स एसिलीकरण (Friedel–Crafts acylation) है। AlCl3 की उपस्थिति में CH3CO+ (एसीलियम आयन) बनता है, जो बेंजीन रिंग पर जुड़कर एसीटोफिनोन बनाता है।
(ii) LiAlH4 एक शक्तिशाली अपचायक है। यह कार्बोक्सिलिक अम्ल (–COOH) को पूरी तरह घटाकर प्राथमिक ऐल्कोहॉल (1° alcohol) बना देता है। इसलिए एसीटिक अम्ल से एथेनॉल बनता है।
मेडोस्वीट पौधे से संबंधित सुगंधित यौगिकों में सैलिसिलऐल्डिहाइड पाया जाता है, इसलिए इसे “मेडोस्वीट से प्राप्त ऐल्डिहाइड” के रूप में पूछा जाता है।
(ब) ✅ व्याख्या
(i) यह फ्राइडेल–क्राफ्ट्स एसिलीकरण (Friedel–Crafts acylation) है। AlCl3 की उपस्थिति में CH3CO+ (एसीलियम आयन) बनता है, जो बेंजीन रिंग पर जुड़कर एसीटोफिनोन बनाता है।
(ii) LiAlH4 एक शक्तिशाली अपचायक है। यह कार्बोक्सिलिक अम्ल (–COOH) को पूरी तरह घटाकर प्राथमिक ऐल्कोहॉल (1° alcohol) बना देता है। इसलिए एसीटिक अम्ल से एथेनॉल बनता है।
क्या आप जानते हैं? 🤔📌
सैलिसिलऐल्डिहाइड
की संरचना में
–OH
और
–CHO
एक ही बेंजीन रिंग पर होते हैं, और
–OH ortho
स्थिति पर होता है।
NaBH4 आमतौर पर कार्बोक्सिलिक अम्ल को नहीं घटाता, लेकिन LiAlH4 घटा देता है, इसलिए परीक्षा में यह फर्क अक्सर पूछा जाता है।
NaBH4 आमतौर पर कार्बोक्सिलिक अम्ल को नहीं घटाता, लेकिन LiAlH4 घटा देता है, इसलिए परीक्षा में यह फर्क अक्सर पूछा जाता है।
17)
(अ) इलेक्ट्रोड विभव को परिभाषित कीजिए।
(ब) ईंधन सेल का नामांकित चित्र बनाइए।
(स) CuSO4 के विलयन को 1 A धारा से 15 मिनट तक वैद्युत अपघटित किया गया। कैथोड पर निक्षेपित Cu का द्रव्यमान ज्ञात कीजिए। (1F = 96500 C mol−1)
(अ) इलेक्ट्रोड विभव को परिभाषित कीजिए।
(ब) ईंधन सेल का नामांकित चित्र बनाइए।
(स) CuSO4 के विलयन को 1 A धारा से 15 मिनट तक वैद्युत अपघटित किया गया। कैथोड पर निक्षेपित Cu का द्रव्यमान ज्ञात कीजिए। (1F = 96500 C mol−1)
उत्तर ✅
(अ)
✅ इलेक्ट्रोड विभव (Electrode Potential) की परिभाषा
किसी इलेक्ट्रोड का इलेक्ट्रोड विभव वह विभवांतर है जो इलेक्ट्रोड और उसके आयनों वाले विलयन (electrolyte) के बीच साम्य पर प्राप्त होता है, जब इलेक्ट्रोड को उसी के आयन वाले विलयन में डुबोया जाता है। ✅
(यही प्रवृत्ति बताता है कि इलेक्ट्रोड इलेक्ट्रॉन देने या लेने की कितनी क्षमता रखता है।)
(ब) ✅ ईंधन सेल (Fuel Cell) का नामांकित चित्र
Fuel cell (H2–O2 cell) का नामांकित चित्र
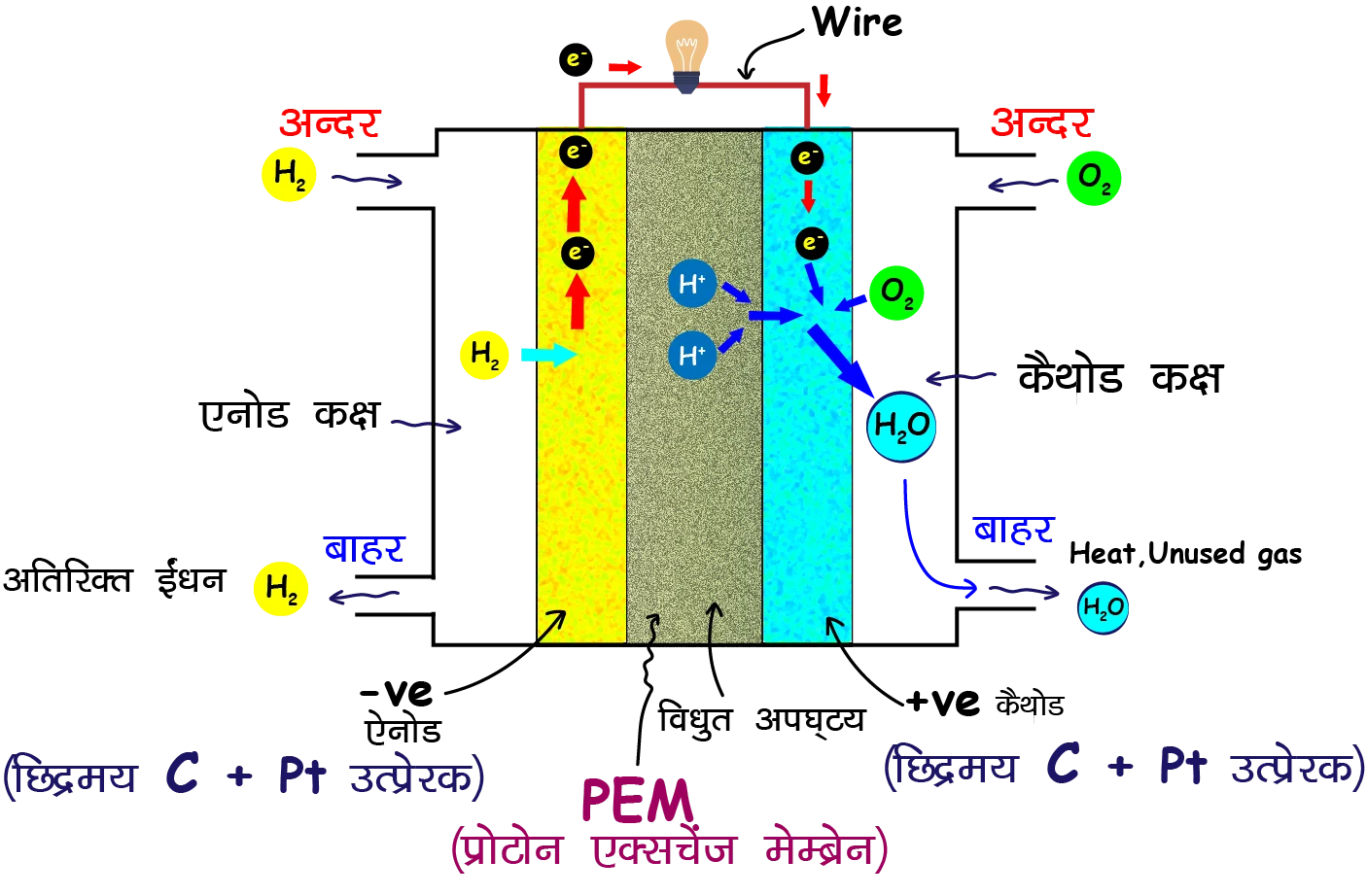
:
Anode (Pt): H2 गैस प्रवेश
Cathode (Pt): O2 गैस प्रवेश
Electrolyte: KOH/क्षारीय विलयन (अक्सर)
Electron flow: बाहरी परिपथ में anode → cathode
Ion flow (OH−): electrolyte में cathode → anode
Overall product: H2O
(स) ✅ कैथोड पर निक्षेपित कॉपर का द्रव्यमान

✅ अंतिम उत्तर
कैथोड पर निक्षेपित कॉपर का द्रव्यमान ≈ 0.296 g (लगभग 0.30 g ) ✅
किसी इलेक्ट्रोड का इलेक्ट्रोड विभव वह विभवांतर है जो इलेक्ट्रोड और उसके आयनों वाले विलयन (electrolyte) के बीच साम्य पर प्राप्त होता है, जब इलेक्ट्रोड को उसी के आयन वाले विलयन में डुबोया जाता है। ✅
(यही प्रवृत्ति बताता है कि इलेक्ट्रोड इलेक्ट्रॉन देने या लेने की कितनी क्षमता रखता है।)
(ब) ✅ ईंधन सेल (Fuel Cell) का नामांकित चित्र
Fuel cell (H2–O2 cell) का नामांकित चित्र

:
Anode (Pt): H2 गैस प्रवेश
Cathode (Pt): O2 गैस प्रवेश
Electrolyte: KOH/क्षारीय विलयन (अक्सर)
Electron flow: बाहरी परिपथ में anode → cathode
Ion flow (OH−): electrolyte में cathode → anode
Overall product: H2O
(स) ✅ कैथोड पर निक्षेपित कॉपर का द्रव्यमान

✅ अंतिम उत्तर
कैथोड पर निक्षेपित कॉपर का द्रव्यमान ≈ 0.296 g (लगभग 0.30 g ) ✅
व्याख्या देखें 👉
इलेक्ट्रोड विभव
को साम्य अवस्था में इलेक्ट्रोड और उसके आयन-विलयन के बीच बनने वाले
विभवांतर
से समझा जाता है, और
H2–O2 fuel cell
में इलेक्ट्रॉन बाहरी परिपथ से
anode → cathode
जाते हैं, जबकि आयन इलेक्ट्रोलाइट में प्रवाहित होते हैं।
वैद्युत अपघटन में निक्षेपित द्रव्यमान प्रवाहित आवेश (Q = It) और समतुल्य भार पर निर्भर करता है।
क्या आप जानते हैं? 🤔📌
समान धारा और समय पर निक्षेपित द्रव्यमान
समतुल्य भार (Equivalent weight = M/n)
के अनुपात में होता है।
अथवा
17)
(अ) सेल विभव को परिभाषित कीजिए।
(ब) मानक हाइड्रोजन इलेक्ट्रोड का नामांकित चित्र बनाइए।
(स) 298 K पर 0.100 M KCl विलयन की चालकता 0.0129 S cm−1 है। 0.100 M KCl विलयन की मोलर चालकता की गणना कीजिए।
(अ) सेल विभव को परिभाषित कीजिए।
(ब) मानक हाइड्रोजन इलेक्ट्रोड का नामांकित चित्र बनाइए।
(स) 298 K पर 0.100 M KCl विलयन की चालकता 0.0129 S cm−1 है। 0.100 M KCl विलयन की मोलर चालकता की गणना कीजिए।
उत्तर ✅
(अ)
✅ सेल विभव (Cell Potential) की परिभाषा
सेल विभव वह विभवांतर है जो किसी विद्युत रासायनिक सेल के कैथोड और एनोड के बीच उत्पन्न होता है। इसे सेल के दोनों इलेक्ट्रोडों के विभवों के अंतर के रूप में लिखा जाता है:
Ecell = Ecathode − Eanode ✅
(ब) ✅ मानक हाइड्रोजन इलेक्ट्रोड (SHE) का नामांकन :
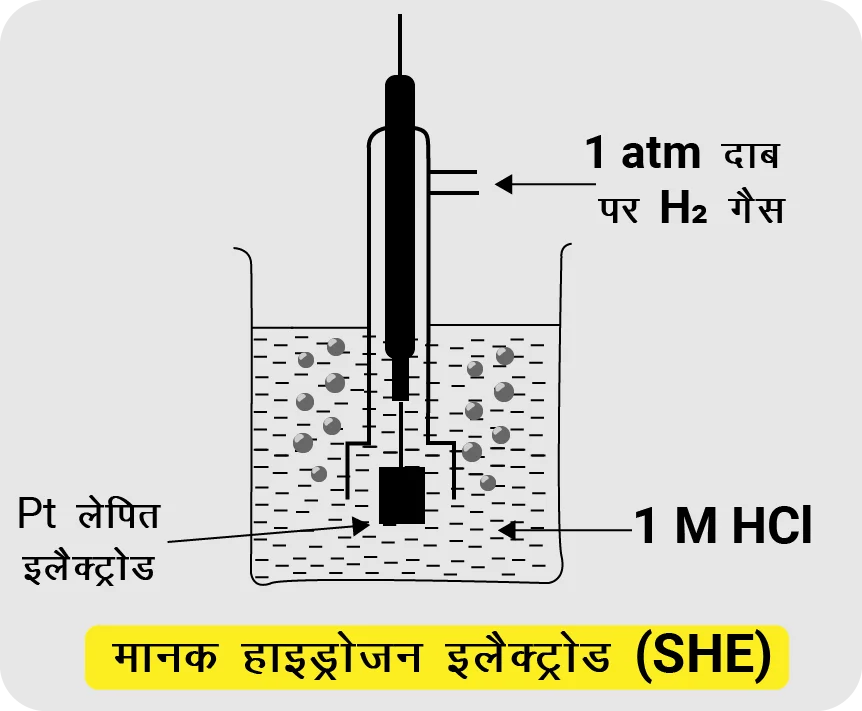
प्लैटिनम (Pt) इलेक्ट्रोड (Pt black coated)
H2 गैस का प्रवाह 1 atm पर
H+ आयन वाला विलयन (आम तौर पर 1 M HCl)
तापमान 298 K (25°C)
गैस इनलेट/आउटलेट
आधी अभिक्रिया: 2H+ + 2e− ⇌ H2(g)
मानक इलेक्ट्रोड विभव: 0.00 V (मानक अवस्था में)
(स) ✅ 0.100 M KCl की मोलर चालकता (Molar Conductivity)
दिया है:
κ (चालकता) = 0.0129 S cm−1
C = 0.100 M
सूत्र: Λm = (κ × 1000) / C
(यहाँ κ की इकाई S cm−1 हो तो Λm की इकाई S cm2 mol−1 आती है)
मान रखें:
Λm = (0.0129 × 1000) / 0.100
Λm = 12.9 / 0.100
Λm = 129 S cm2 mol−1 ✅
✅ अंतिम उत्तर
0.100 M KCl विलयन की मोलर चालकता = 129 S cm2 mol−1 (298 K पर) ✅
सेल विभव वह विभवांतर है जो किसी विद्युत रासायनिक सेल के कैथोड और एनोड के बीच उत्पन्न होता है। इसे सेल के दोनों इलेक्ट्रोडों के विभवों के अंतर के रूप में लिखा जाता है:
Ecell = Ecathode − Eanode ✅
(ब) ✅ मानक हाइड्रोजन इलेक्ट्रोड (SHE) का नामांकन :

प्लैटिनम (Pt) इलेक्ट्रोड (Pt black coated)
H2 गैस का प्रवाह 1 atm पर
H+ आयन वाला विलयन (आम तौर पर 1 M HCl)
तापमान 298 K (25°C)
गैस इनलेट/आउटलेट
आधी अभिक्रिया: 2H+ + 2e− ⇌ H2(g)
मानक इलेक्ट्रोड विभव: 0.00 V (मानक अवस्था में)
(स) ✅ 0.100 M KCl की मोलर चालकता (Molar Conductivity)
दिया है:
κ (चालकता) = 0.0129 S cm−1
C = 0.100 M
सूत्र: Λm = (κ × 1000) / C
(यहाँ κ की इकाई S cm−1 हो तो Λm की इकाई S cm2 mol−1 आती है)
मान रखें:
Λm = (0.0129 × 1000) / 0.100
Λm = 12.9 / 0.100
Λm = 129 S cm2 mol−1 ✅
✅ अंतिम उत्तर
0.100 M KCl विलयन की मोलर चालकता = 129 S cm2 mol−1 (298 K पर) ✅
व्याख्या देखें 👉
सेल विभव
को इलेक्ट्रोड विभवों के अंतर से लिखा जाता है, जबकि
मोलर चालकता
निकालते समय
κ
और
C
का सही यूनिट रूपांतरण जरूरी होता है।
क्या आप जानते हैं? 🤔📌
मानक हाइड्रोजन इलेक्ट्रोड
का मानक इलेक्ट्रोड विभव
0.00 V
माना जाता है, इसलिए दूसरे इलेक्ट्रोडों के विभव इसी के सापेक्ष मापे जाते हैं।
18)
(अ) सरल ईथर का कोई एक उदाहरण लिखिए।
(ब) प्रोपीन के अम्ल उत्प्रेरित जलयोजन (Acid catalysed hydration) की क्रियाविधि समझाइए।
(अ) सरल ईथर का कोई एक उदाहरण लिखिए।
(ब) प्रोपीन के अम्ल उत्प्रेरित जलयोजन (Acid catalysed hydration) की क्रियाविधि समझाइए।
उत्तर ✅
(अ)
✅ उत्तर
सरल ईथर का उदाहरण: डाइएथिल ईथर (C2H5–O–C2H5) ✅
(इसे इथॉक्सीइथेन भी कहते हैं।)
(ब) ✅ प्रोपीन का अम्ल उत्प्रेरित जलयोजन: क्रियाविधि (Mechanism)
अभिक्रिया :
CH3–CH=CH2 + H2O —(H+)→ CH3–CH(OH)–CH3
✅ मुख्य उत्पाद: 2-प्रोपेनॉल (आइसोप्रोपिल अल्कोहॉल)
चरण 1: प्रोटोनन (Protonation) और कार्बोकैटायन बनना
अम्ल से H+ डबल बॉन्ड पर जुड़ता है। प्रोपीन में H+ टर्मिनल कार्बन (CH2) पर जुड़ता है ताकि अधिक स्थिर द्वितीयक कार्बोकैटायन बने:
CH3–CH=CH2 + H+ → CH3–C+H–CH3
👉 यह मार्कोवनीकॉव नियम के अनुसार होता है (अधिक स्थिर कार्बोकैटायन बनता है) ।
चरण 2: जल का नाभिकरागी आक्रमण (Nucleophilic attack by water)
अब H2O (नाभिकरागी) इस कार्बोकैटायन पर आक्रमण करता है और ऑक्सोनियम आयन बनता है:
CH3–C+H–CH3 + H2O → CH3–CH(OH2+)–CH3
चरण 3: डी-प्रोटोनन (Deprotonation) और अल्कोहॉल बनना
ऑक्सोनियम आयन से एक H+ निकल जाता है (अम्ल वापस बन जाता है) और अंतिम उत्पाद मिलता है:
CH3–CH(OH2+)–CH3 → CH3–CH(OH)–CH3 + H+
✅ उत्पाद: 2-प्रोपेनॉल
सरल ईथर का उदाहरण: डाइएथिल ईथर (C2H5–O–C2H5) ✅
(इसे इथॉक्सीइथेन भी कहते हैं।)
(ब) ✅ प्रोपीन का अम्ल उत्प्रेरित जलयोजन: क्रियाविधि (Mechanism)
अभिक्रिया :
CH3–CH=CH2 + H2O —(H+)→ CH3–CH(OH)–CH3
✅ मुख्य उत्पाद: 2-प्रोपेनॉल (आइसोप्रोपिल अल्कोहॉल)
चरण 1: प्रोटोनन (Protonation) और कार्बोकैटायन बनना
अम्ल से H+ डबल बॉन्ड पर जुड़ता है। प्रोपीन में H+ टर्मिनल कार्बन (CH2) पर जुड़ता है ताकि अधिक स्थिर द्वितीयक कार्बोकैटायन बने:
CH3–CH=CH2 + H+ → CH3–C+H–CH3
👉 यह मार्कोवनीकॉव नियम के अनुसार होता है (अधिक स्थिर कार्बोकैटायन बनता है) ।
चरण 2: जल का नाभिकरागी आक्रमण (Nucleophilic attack by water)
अब H2O (नाभिकरागी) इस कार्बोकैटायन पर आक्रमण करता है और ऑक्सोनियम आयन बनता है:
CH3–C+H–CH3 + H2O → CH3–CH(OH2+)–CH3
चरण 3: डी-प्रोटोनन (Deprotonation) और अल्कोहॉल बनना
ऑक्सोनियम आयन से एक H+ निकल जाता है (अम्ल वापस बन जाता है) और अंतिम उत्पाद मिलता है:
CH3–CH(OH2+)–CH3 → CH3–CH(OH)–CH3 + H+
✅ उत्पाद: 2-प्रोपेनॉल
व्याख्या देखें 👉
यह अभिक्रिया
कार्बोकैटायन
के माध्यम से होती है, इसलिए
मार्कोवनीकॉव नियम
के अनुसार अधिक स्थिर कार्बोकैटायन बनता है और वही मुख्य उत्पाद देता है।
क्या आप जानते हैं? 🤔📌
जिस ईथर के दोनों ओर एक जैसे अल्किल समूह हों उसे
सरल (symmetrical/simple) ईथर
कहते हैं।
यह अभिक्रिया कार्बोकैटायन के माध्यम से होती है, इसलिए कभी-कभी पुनर्व्यवस्था (rearrangement) की संभावना भी हो सकती है (दूसरे अल्कीनों में)।
प्रोपीन में मुख्य उत्पाद मार्कोवनीकॉव उत्पाद ही मिलता है: 2-प्रोपेनॉल ।
अथवा
18)
(अ) मिश्रित ईथर का कोई एक उदाहरण लिखिए।
(ब) प्रोपेन-2-ऑल के निर्जलीन (Dehydration) की क्रियाविधि को समझाइए।
(अ) मिश्रित ईथर का कोई एक उदाहरण लिखिए।
(ब) प्रोपेन-2-ऑल के निर्जलीन (Dehydration) की क्रियाविधि को समझाइए।
उत्तर ✅
(अ)
✅ उत्तर
मिश्रित ईथर का उदाहरण: मेथॉक्सीएथेन (CH3–O–CH2CH3) ✅
(इसे इथाइल मेथाइल ईथर भी कहते हैं।)
(ब) ✅ प्रोपेन-2-ऑल का निर्जलीन: क्रियाविधि (Mechanism)
प्रोपेन-2-ऑल (CH3–CH(OH)–CH3) को सं. H2SO4/H3PO4 और ऊष्मा देने पर निर्जलीन होकर प्रोपीन (Propene) बनता है। यह अभिक्रिया सामान्यतः E1 (कार्बोकैटायन) तंत्र से होती है।
समग्र अभिक्रिया:
CH3–CH(OH)–CH3 —(conc. H2SO4, 443 K)→ CH3–CH=CH2 + H2O
✅ मुख्य उत्पाद: प्रोपीन
चरण 1: प्रोटोनन (Protonation)
अम्ल से H+ अल्कोहॉल के ऑक्सीजन पर जुड़ता है, जिससे –OH एक अच्छा leaving group बन जाता है:
CH3–CH(OH)–CH3 + H+ → CH3–CH(OH2+)–CH3
चरण 2: जल का निकलना (Leaving of water) और कार्बोकैटायन बनना
अब H2O निकल जाता है और द्वितीयक कार्बोकैटायन बनता है:
CH3–CH(OH2+)–CH3 → CH3–C+H–CH3 + H2O
चरण 3: डी-प्रोटोनन (Deprotonation) और अल्कीन बनना
अम्ल का संयुग्मी क्षार (जैसे HSO4− ) पास के कार्बन से β-हाइड्रोजन निकाल लेता है और डबल बॉन्ड बन जाता है:
CH3–C+H–CH3 → CH3–CH=CH2 + H+
✅ उत्पाद: प्रोपीन और H+ वापस बन जाता है (अम्ल उत्प्रेरक है) ।
मिश्रित ईथर का उदाहरण: मेथॉक्सीएथेन (CH3–O–CH2CH3) ✅
(इसे इथाइल मेथाइल ईथर भी कहते हैं।)
(ब) ✅ प्रोपेन-2-ऑल का निर्जलीन: क्रियाविधि (Mechanism)
प्रोपेन-2-ऑल (CH3–CH(OH)–CH3) को सं. H2SO4/H3PO4 और ऊष्मा देने पर निर्जलीन होकर प्रोपीन (Propene) बनता है। यह अभिक्रिया सामान्यतः E1 (कार्बोकैटायन) तंत्र से होती है।
समग्र अभिक्रिया:
CH3–CH(OH)–CH3 —(conc. H2SO4, 443 K)→ CH3–CH=CH2 + H2O
✅ मुख्य उत्पाद: प्रोपीन
चरण 1: प्रोटोनन (Protonation)
अम्ल से H+ अल्कोहॉल के ऑक्सीजन पर जुड़ता है, जिससे –OH एक अच्छा leaving group बन जाता है:
CH3–CH(OH)–CH3 + H+ → CH3–CH(OH2+)–CH3
चरण 2: जल का निकलना (Leaving of water) और कार्बोकैटायन बनना
अब H2O निकल जाता है और द्वितीयक कार्बोकैटायन बनता है:
CH3–CH(OH2+)–CH3 → CH3–C+H–CH3 + H2O
चरण 3: डी-प्रोटोनन (Deprotonation) और अल्कीन बनना
अम्ल का संयुग्मी क्षार (जैसे HSO4− ) पास के कार्बन से β-हाइड्रोजन निकाल लेता है और डबल बॉन्ड बन जाता है:
CH3–C+H–CH3 → CH3–CH=CH2 + H+
✅ उत्पाद: प्रोपीन और H+ वापस बन जाता है (अम्ल उत्प्रेरक है) ।
व्याख्या देखें 👉
E1
तंत्र में पहले
कार्बोकैटायन
बनता है, इसलिए निर्जलीन की गति कार्बोकैटायन की स्थिरता पर निर्भर करती है।
क्या आप जानते हैं? 🤔📌
जिस ईथर में दोनों तरफ अलग-अलग अल्किल समूह हों उसे
मिश्रित (unsymmetrical/mixed) ईथर
कहते हैं।
3° > 2° > 1° अल्कोहॉल निर्जलीन में (E1) आमतौर पर तेजी से प्रतिक्रिया करते हैं, क्योंकि कार्बोकैटायन की स्थिरता इसी क्रम में बढ़ती है।
प्रोपेन-2-ऑल से मुख्यतः प्रोपीन ही बनता है (यहाँ rearrangement की जरूरत नहीं पड़ती)।
